Cómo gestionar la vaporización en los sistemas de muestreo

Cómo gestionar la vaporización en los sistemas de muestreo
Jon Kestner
No es fácil vaporizar una muestra, ni siempre es posible. Sin embargo, si el analizador de su sistema de muestreo analítico requiere gas, pero la muestra es líquida, la única opción es convertir el líquido en gas. Este proceso se llama vaporización o vaporización flash. El objetivo es convertir una muestra de todo líquido en vapor instantáneamente sin cambiar la composición.
Si continúa con la vaporización, es importante comprender la diferencia entre evaporación y vaporización. La evaporación se produce gradualmente con un aumento de la temperatura. La vaporización ocurre instantáneamente con una caída de presión.
No es posible vaporizar una muestra aumentando la temperatura. El calor provoca la evaporación, y agregar más calor simplemente hace que la evaporación ocurra más rápido. En una muestra mixta, la evaporación permitirá que algunos compuestos se evaporen antes que otros, dando como resultado el fraccionamiento. La vaporización, cuando se hace correctamente, asegura que todos los compuestos se vaporicen al mismo tiempo, preservando la composición de la muestra.
Las cosas podrían salir mal al vaporizar. En lugar de convertir toda la muestra en un vapor, sin querer podría causar una combinación de vaporización y evaporación, lo que resultaría en un fraccionamiento. Una vez que se fracciona una muestra de compuestos mixtos, ya no es adecuada para el análisis.
Con el fraccionamiento, un escenario común es que las moléculas más ligeras se evaporen primero y viajen hacia el analizador, mientras que las moléculas más pesadas permanecen en la fase líquida. Incluso si en algún punto posterior del proceso una muestra fraccionada parece ser todo gas, la mezcla no tendrá las mismas proporciones moleculares que tenía antes del fraccionamiento. Ya no representará con precisión el producto tomado de la línea de proceso. El ajuste de las variables del proceso (temperatura, presión y flujo) puede ayudar a garantizar una vaporización adecuada y un resultado analítico preciso.
Comprender la vaporización
Para vaporizar una muestra, normalmente se utiliza un regulador de vaporización, también llamado vaporizador. Un vaporizador es un regulador reductor de presión con la capacidad de transferir calor a la muestra en el lugar correcto. La vaporización consiste en un proceso de tres etapas, como se ve en el diagrama a continuación. Primero, la muestra ingresa al regulador de vaporización como líquido. En este punto, el líquido no debe estar hirviendo.
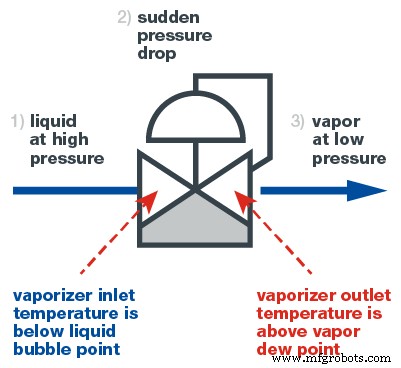
Segundo, el líquido pasa a través de la cavidad reguladora en el regulador de vaporización, lo que resulta en una caída de presión severa y repentina que vaporiza el líquido. Al mismo tiempo, se aplica calor, lo que permite que el líquido vaporizado siga siendo vapor.
Tercero, la muestra, ahora un gas, sale del regulador de vaporización y viaja al analizador para ser leída. Debido a la transición inmediata a la fase de vapor, la composición del gas no cambia con respecto a la del líquido, lo que garantiza una lectura precisa.
En este delicado proceso, existen muchas variables o insumos que determinan el éxito o el fracaso. A los efectos de esta discusión, nos centraremos en dos conjuntos principales de entradas.
El primer conjunto de entradas se relaciona con la composición de la muestra. Dependiendo de su composición, la muestra comenzará a burbujear y terminará de vaporizarse a diferentes presiones y temperaturas. Necesitaremos saber cuáles son estas presiones y temperaturas para gestionar con éxito el proceso.
El segundo conjunto de entradas se refiere a la configuración que usted controla en su sistema de muestreo:presión, temperatura y caudal. La presión y la temperatura se controlan en el vaporizador, mientras que el flujo se controla aguas abajo en un rotámetro (caudalímetro de área variable) y una válvula de aguja. Estas entradas se establecen en función de lo que sabemos sobre el primer conjunto de entradas. La vaporización adecuada requiere un delicado equilibrio de cada entrada. Incluso cuando se aborda la vaporización de una manera sistemática como esta, el proceso requiere algo de ensayo y error.
Comprender la muestra
La mejor manera de comprender el primer conjunto de entradas es con un diagrama de fase. Un diagrama de fase traza la presión y la temperatura, mostrando en cualquier par de condiciones si una sustancia será vapor, líquido o sólido. Las líneas indican las interfaces entre dos fases.
El siguiente gráfico representa un diagrama de fase para 20 por ciento de hexano en pentano. Cuando la muestra está por encima del punto de burbuja (línea azul), es todo líquido. La muestra debe estar completamente líquida cuando entre al vaporizador. Cuando la mezcla está por debajo del punto de rocío (línea dorada), todo es vapor. La muestra debe ser todo vapor cuando sale del vaporizador.
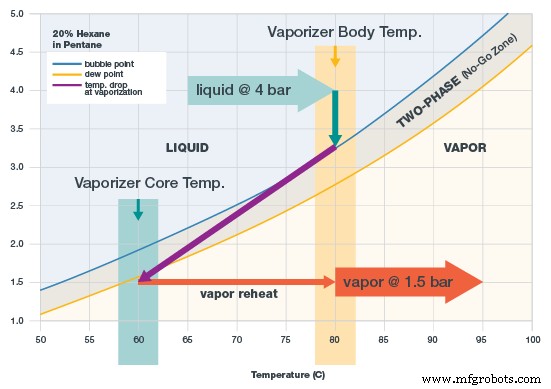
Diagrama de fase que muestra 20 por ciento de hexano en pentano, con ajustes de temperatura
Entre las líneas del punto de burbujeo y el punto de rocío se encuentra el rango de ebullición, o “zona prohibida” de la muestra. Aquí, la mezcla está en dos fases:parte líquida y parte vapor. Una vez que una muestra cae dentro de este rango, se fracciona y ya no es adecuada para el análisis.
Con muestras puras y casi puras, hay poco o ningún rango de ebullición. Las líneas del punto de burbuja y del punto de rocío están casi superpuestas una encima de la otra. Las muestras puras y casi puras se convertirán en vapor de la misma composición, ya sea por evaporación o vaporización. Algunas muestras industriales se acercan a este nivel de pureza y se convierten fácilmente.
Por otro lado, algunas muestras tienen un rango de ebullición tan amplio que no pueden vaporizarse con éxito. No hay forma de pasar del lado líquido al lado vapor del rango de ebullición. Las variables temperatura, flujo y presión no se pueden alterar para evitar el fraccionamiento.
La mayoría de las muestras se encuentran entre estos dos extremos. Por ejemplo, en el diagrama de fase de la muestra, la banda entre el punto de burbujeo y el punto de rocío es lo suficientemente estrecha como para que, con los ajustes adecuados, la muestra pueda pasar efectivamente del lado líquido al lado del vapor del rango de ebullición. Al mismo tiempo, la banda de entrada es lo suficientemente amplia como para que las variables deban modificarse cuidadosamente para evitar tener una muestra en el rango de ebullición.
Configuración de temperatura, presión y caudal
La vaporización es un acto de equilibrio entre las variables. El siguiente es un proceso de cuatro pasos para configurar entradas para su temperatura, presión y flujo.
- Determine la presión de entrada en el vaporizador. Esta presión, que es fija, es la presión del proceso, siempre que el vaporizador esté ubicado cerca del grifo de muestra. Una presión más alta es mejor porque permite una temperatura del vaporizador más alta, sin hervir el líquido entrante.
-
Establezca la temperatura de entrada. Hay dos objetivos al ajustar la temperatura. Primero, la temperatura debe ser lo suficientemente baja para que cuando la muestra ingrese al vaporizador sea completamente líquida y no burbujee. En el diagrama de fase de 20 por ciento de hexano en pentano, el punto de burbujeo a 4 bar es 88°C. Para permitir un margen de error en el mantenimiento del estado líquido, elija 80 °C.
El segundo objetivo es que la temperatura debe ser lo suficientemente alta para contribuir a la vaporización de la muestra. Cuando vaporizas la muestra, la temperatura desciende, de acuerdo con las leyes de conservación de la energía. La temperatura de la muestra debe ser lo suficientemente alta desde el principio para que, después de la caída de presión, la muestra no esté en el rango de ebullición.
- Establece la presión de salida en el vaporizador. El objetivo es dejar caer la presión por debajo de la línea del punto de rocío de oro. En el diagrama de fase de ejemplo, la presión de salida se establece en 1,5 bar. Si la presión de salida fuera más alta en este ejemplo, la muestra no se vaporizaría por completo ni se fraccionaría.
- Establezca el flujo. El flujo se establece aguas abajo en una válvula y un rotámetro, no en el vaporizador. En un sistema de muestreo, es deseable un alto flujo de vapor porque mueve la muestra al analizador más rápido. Sin embargo, el alto flujo también puede ser problemático, porque se requiere más calor para vaporizar la muestra. En otras palabras, un alto flujo da como resultado una mayor caída de temperatura en el momento de la vaporización. En el diagrama de fase de ejemplo, la línea morada ilustra la caída de temperatura. A medida que aumenta el flujo, la línea morada se inclina más hacia la izquierda.
Otra variable que influye en la caída de temperatura es la capacidad de transferencia de calor del vaporizador. Algunos vaporizadores están construidos para que el calor se transfiera más eficientemente a la muestra. Cuando la muestra líquida se convierte en vapor y su temperatura desciende, extrae calor del acero inoxidable que la rodea. La pregunta crítica es qué tan eficientemente el vaporizador puede reemplazar ese calor y mantenerlo fluyendo hacia la muestra. Cuanto más calor pueda extraer la muestra, menos caerá su temperatura durante la vaporización.
En algunos casos, es posible que el vaporizador esté caliente al tacto por fuera pero frío por dentro. Esto se debe a que la muestra vaporizada consume mucho calor y el vaporizador no puede transferir suficiente calor para mantenerse al día. La mejor solución es reducir el caudal.
La vaporización implica cierta aproximación. Los ingenieros de Swagelok Field Service pueden ayudar a su equipo a determinar los vaporizadores adecuados para su sistema de muestreo específico. Como regla general, mantenga el caudal lo más bajo posible sin causar un retraso inaceptable en el tiempo de viaje de la muestra al analizador. Es mejor comenzar con un caudal bajo y experimentar aumentándolo que comenzar con un caudal más alto.
Solución de problemas
Los diagramas de fase ayudan a aproximar los ajustes de temperatura, presión y flujo, pero aún será necesario solucionar algunos problemas. Una indicación segura de un problema es la mala repetibilidad de los resultados del analizador. A continuación, presentamos dos posibilidades cuando la muestra se fracciona en lugar de vaporizarse, siendo el problema n.° 1 el más común:
Problema #1
Solo una parte de la muestra se vaporiza. El líquido pasa a través del vaporizador y permanece en la tubería del lado aguas abajo. Eventualmente, se evapora y extrae calor de la tubería circundante, lo que hace que la tubería se enfríe al tacto o que se forme escarcha o hielo. El líquido aguas abajo del vaporizador puede pasar más allá del área del regulador y hacia otros componentes, como medidores de flujo y filtros, donde puede causar daños considerables.
Solución n.º 1
Problema #2
La muestra está hirviendo a la entrada del vaporizador. Se fracciona antes de que pueda vaporizarse. Un indicador de este problema es que el tubo de entrada al vaporizador se contrae, a veces violentamente, y los valores de medición oscilan. Las moléculas más ligeras se evaporan y producen una gran nube de moléculas de vapor. Algunas de estas moléculas más ligeras pasan al analizador, dando un análisis inexacto. El resto crea una "pared de vapor", que empuja el líquido de regreso al proceso. Una parte de esa pared de vapor luego se enfría y se condensa. Finalmente, la muestra líquida se mueve nuevamente hacia el vaporizador, donde las moléculas más ligeras se evaporan, comenzando el ciclo nuevamente. Eventualmente, las moléculas más pesadas llegan al vaporizador y se mueven hacia el analizador dando un análisis completamente diferente.
Solución n.º 2
Para resolver este problema, baje la temperatura del vaporizador.
Conclusión
Vaporizar una muestra líquida es un desafío. En muchos sistemas de muestreo de todo el mundo, los vaporizadores fraccionan muestras constantemente y envían muestras no representativas al analizador. Puede aumentar drásticamente sus posibilidades de éxito utilizando un diagrama de fase de la mezcla particular de compuestos de su sistema. Puede aumentar aún más su tasa de éxito al comprender lo que está ocurriendo en el proceso; específicamente, al saber cuáles son las variables (temperatura, presión y flujo) y al comprender su papel en la influencia del resultado del proceso. Con este marco en su lugar, puede alcanzar la configuración correcta, ajustándose de acuerdo con los signos y síntomas que observe.
Tecnología Industrial
- Cómo se benefician los fabricantes de la convergencia de TI y TO
- Cómo gestionar el cierre de una planta
- Cómo los datos están habilitando la cadena de suministro del futuro
- Cómo administrar su departamento de adquisiciones de forma remota
- ¿Cómo funcionan los sistemas SCADA?
- Cómo lograr una alta disponibilidad en los sistemas de control modernos
- Cómo usar la IA perimetral para administrar su negocio hacia una mejor normalidad
- Cómo gestionar los riesgos de seguridad del almacén
- ¿Cómo pueden los gerentes de fábrica gestionar sus residuos de manera eficiente?
- Cómo mitigar y administrar su fábrica después de un accidente
- Temperatura de PCB:una guía sobre cómo manejar las altas temperaturas



