Andamios de fibroína de seda cargados con proteína morfogénica ósea-2 (rhBMP2) para mejorar la osteoinductividad en la ingeniería de tejidos óseos
Resumen
Existe una demanda creciente de formulaciones de andamios de fibroína de seda (SF) en aplicaciones biomédicas. SF se reticuló mediante glutaraldehído con proteína morfogénica ósea humana recombinante osteoinductora-2 (rhBMP2) de diferentes proporciones, a saber. (i) 3% SF sin rhBMP2 (SF), (ii) 3% SF con la misma cantidad de rhBMP2 (SF + BMP2) y (iii) 12% SF con 3% de rhBMP2 (4SF + BMP2), y estos Las soluciones se utilizaron en la fabricación de nanoandamios basada en electrohilado para evaluar el potencial osteoinductivo aumentado de los andamios SF con rhBMP2. La relación tensión-deformación sugirió que no hay pérdida en la resistencia mecánica de las fibras con la adición de rhBMP2, y la resistencia mecánica del andamio mejoró con el aumento de la concentración de SF. La asociación rhBMP2 aumentó la capacidad de retención de agua del andamio como es evidente a partir de los estudios de hinchazón. Se encontró que la viabilidad de las hMSCs era mayor en los armazones conjugados y los armazones no exhiben ninguna citotoxicidad hacia las células huésped. Se encontró que las células tenían una mayor actividad de fosfatasa alcalina en armazones conjugados en condiciones in vitro e in vivo, lo que establece la osteoinductividad aumentada de la nueva construcción. Se descubrió que los andamios también son efectivos para la formación de hueso in vivo.
Antecedentes
La capacidad regenerativa del hueso permite la reparación de pequeñas fracturas óseas por sí misma. Se forma el hueso, seguido de la unión y, finalmente, la reconstrucción de la forma original del hueso. Sin embargo, esta capacidad es limitada y esto crea la necesidad de autoinjertos o aloinjertos para el tratamiento [1]. El aloinjerto implica obtener el hueso de un donante separado que puede causar una reacción inmunológica. El autoinjerto, donde el hueso se obtiene del propio cuerpo del paciente, no crea problemas inmunológicos, pero está limitado por la cantidad suficiente de huesos disponibles [2, 3, 4].
La ingeniería de tejidos se percibe como una tecnología potencial para superar la limitación inmunológica del aloinjerto y el autoinjerto. Con la ingeniería de tejidos, se cultivan células especializadas como las células madre mesenquimales humanas o las células de osteosarcoma (MG63) en un entorno adecuado sobre un andamio prefabricado, y este sistema de células y andamio se utiliza luego como injerto [5, 6].
El andamio se utiliza para proporcionar anclaje y nicho bioquímico a las células para su supervivencia y proliferación. Varias propiedades a saber. La resistencia mecánica, osteoinducción, biorreabsorción, porosidad graduada y biocompatibilidad se deben considerar al seleccionar el material para fabricar el andamio. La osteoinducción (inducción de la formación de hueso) es una de las propiedades requeridas del material que se utilizará en la fabricación de andamios de ingeniería de tejido óseo (BTE) [7]. Los andamios con factores osteogénicos son potentes para imitar el proceso de regeneración del tejido óseo que acopla la angiogénesis y la osteogénesis que pueden reclutar células progenitoras y su diferenciación. Las proteínas morfogénicas óseas (BMP) son la clase de factores de crecimiento que inducen la formación de hueso y se proponen para aplicaciones de BTE junto con la matriz ósea desmineralizada (DBM) y el fosfato de calcio [8,9,10].
Varios grupos han informado del uso de metales, cerámicas, polímeros sintéticos y compuestos, y fibroína de seda como materiales potenciales para la fabricación de andamios en BTE. Se ha informado que la fibroína de seda (SF) es un material adecuado para la fabricación de andamios para aplicaciones de ingeniería de tejidos debido a sus notables propiedades mecánicas y biocompatibles [5]. Hasta la fecha, no se ha publicado ningún informe que evalúe los beneficios asociativos de las BMP con nanoandamios de SF electrohilado.
Aquí, informamos la fabricación de nuevos andamios nanofibrosos electrohilados SF conjugado con proteína morfogénica de hueso humano recombinante 2 (rhBMP2). Los armazones se compararon con los de armazones SF puros para dilucidar el efecto de la conjugación de rhBMP2 sobre la osteoinducción. También se midieron la viabilidad celular y las propiedades de proliferación celular para establecer la potencia del andamio para nuevas y mejores aplicaciones de ingeniería de tejidos óseos.
Métodos
Preparación de soluciones acuosas de SF / BMP2
Al principio, SF se aisló de los capullos del gusano de seda, Bombyx mori , como una solución acuosa. Se siguió el protocolo establecido con ligeras modificaciones [11]. Los capullos se hirvieron en 100 ml de Na 2 0,02 M CO 3 durante 20 min y luego enjuague bien con agua destilada para eliminar el exceso de sericina y cera solubles en agua. Después, la fibroína extraída se disolvió en una solución de bromuro de litio 9 M a 60ºC durante 4 horas y se dializó adicionalmente frente a agua durante 4 días. La concentración final se determinó pesando la materia seca después del secado y se encontró que era del 7% w / v . Esta solución se usó luego después de concentrar a diferentes niveles por diálisis contra 1 L de polietilenglicol al 25% (PEG, 10,000 g mol −1 ) solución a temperatura ambiente. Se prepararon soluciones acuosas de SF diluidas diluyéndolas con agua destilada y todas las soluciones se almacenaron a 10 ° C hasta su posterior procesamiento. Se disolvió polvo liofilizado de proteína 2 morfogénica ósea humana recombinante (rhBMP2) en PBS (pH 3,8). La solución de proteína se esterilizó con filtros de jeringa de 0,22 µm y se añadió como solución acuosa a cada solución de fibroína con agitación continua. Se empleó reticulación mediada por glutaraldehído para asociar BMP con fibroína. Brevemente, para 10 ml de mezcla de reacción, 5 ml de cada uno de fibroína de seda al 6% y rhBMP2 al 1% se reticularon usando 200 μL de glutaraldehído y 40 μL, HCl 12 N como agente activador de grupo. Con este procedimiento, se prepararon tres soluciones:(i) 3% de fibroína de seda sin rhBMP2 (SF), (ii) 3% de fibroína de seda con 0,5% de rhBMP2 (SF + rhBMP2) y (iii) 12% de fibroína de seda con 0,125% de rhBMP2 como en (ii) (4SF + rhBMP2). Estas soluciones se utilizaron en procedimientos de electrohilado para la fabricación de andamios.
Fabricación de andamios por electrohilado
Para la fabricación de andamios, cada solución se cargó en una jeringa de vidrio de 5 ml con una aguja de acero inoxidable (25G, DI 0,26 mm, Sigma Aldrich) que está conectada a un suministro de CC de 5,5 kV. Para la preparación de fibras, el caudal de salida se mantuvo a 0,4 ml h −1 utilizando una bomba de jeringa, y las fibras electrohiladas se recogieron en una hoja de aluminio mantenida a un espacio de 15 cm desde la punta del capilar. Las muestras se recolectaron durante 4 h cada una.
Microscopía electrónica de barrido
Para el examen morfológico de los andamios preparados, se realizó SEM utilizando Zeiss EVO40SEM. Las muestras se recubrieron por pulverización catódica con oro antes de que las imágenes escaneadas se procesaran más. La determinación del diámetro de la fibra se realiza promediando los diámetros de 10 fibras aleatorias en el marco de la imagen.
Propiedades mecánicas del andamio
Se realizaron experimentos de compresión para evaluar las propiedades mecánicas de los andamios desarrollados utilizando el comprobador electromecánico de sobremesa de una sola columna Instron (modelo 3345, Instron, Canton, MA). Para determinar la resistencia a la tracción y el alargamiento a la rotura de las curvas tensión-deformación a 25 ° C y 50% de humedad se utilizaron fibras de 0,2 mm de diámetro, obtenidas por electrohilado a mayor duración.
Estudio de hinchazón
Para medir la relación de hinchamiento, cada formulación se disolvió en PBS (pH 7,4) a 37ºC. Se tomaron muestras a intervalos de tiempo predeterminados y se midió el peso seco utilizando una balanza electrónica. La prueba continuó hasta que se alcanzó el peso de equilibrio. La relación de hinchamiento se expresó a continuación:
$$ \ mathrm {Inflamación} \ \ mathrm {ratio} \ left (\% \ right) =\ frac {W \ mathrm {s} -W \ mathrm {o}} {W \ mathrm {o}} $$donde, W o =peso seco inicial de las matrices nanofibrosas y W s =peso de las matrices nanofibrosas hinchadas en cada momento.
Cultivo celular
En el presente estudio se utilizaron células madre mesenquimales humanas (hMSC) para evaluar el potencial osteoinductivo de los nanoandamios fabricados. Las hMSC se cultivaron y mantuvieron en DMEM con suero de ternero fetal al 10% y penicilina al 1%, a 37 ° C en CO 2 al 5% atmósfera humidificada hasta que se logró una confluencia del 90%. Luego, las células se tripsinizaron, centrifugaron y resuspendieron en medio para su cuantificación.
Los andamios se esterilizaron lavándolos con etanol e irradiando con luz UV durante 30 minutos y después se lavaron con PBS (pH 7,4). Se administra un tratamiento con DMEM a los andamios antes de la siembra celular. Se añadieron gota a gota 20 µl de suspensión celular a cada andamio y película plástica que sirvió de control. Los andamios se mantuvieron en reposo en atmósfera humidificada (37 ° C, 5% CO 2 ) durante 30 min. Luego, los andamios se incubaron en DMEM durante 21 días con reposición regular de medio cada día alterno.
Ensayo de adhesión celular
Para evaluar la capacidad de adhesión de las células con el andamio, se contó el número de células no adheridas después de 1, 3 y 6 h de siembra inicial según el método de la literatura con ligeras modificaciones [6]. Se recogió el medio celular y se realizó el recuento celular con un hemocitómetro. La diferencia entre el recuento de siembra inicial y el número de células no adheridas se consideró como el número de células adheridas. Los resultados se expresaron en términos de porcentaje de adhesión según la siguiente ecuación:
$$ \% \ mathrm {Adhesión} =\ frac {\ mathrm {Inicial} \ \ mathrm {siembra} - \ mathrm {número} \ \ mathrm {de} \ \ mathrm {no} \ \ mathrm {adherente} \ kern0 .5em \ mathrm {celdas}} {\ mathrm {Inicial} \ \ mathrm {siembra}} \ veces 100 $$Ensayo de citotoxicidad
Para medir el efecto tóxico de las matrices nanofibrosas, se realizó el ensayo MTT. Después del período de tiempo respectivo, las construcciones se incubaron en solución MTT (1 mg mL −1 solución madre diluida en PBS (pH 7,4) en una proporción de 1:10) y se incubó durante 4 h. Las células viables convierten el MTT en sal de formazán durante este período de incubación. La sal de formazán se disolvió mediante la adición de DMSO y se mantuvo a un lado durante 20 min. La absorbancia que se origina en la sal de formazán se midió cuantitativamente registrando los cambios en la absorbancia a 570 nm utilizando un lector de microplacas.
Ensayo de proliferación celular
Se realizó un ensayo de reducción de colorante azul Alamar (AB) para determinar la proliferación de células dentro del andamio. Los andamios se incubaron en tinte diluido con DMEM durante 4 h, y la reducción del tinte se midió espectrofotométricamente. El porcentaje de reducción de AB se calculó como:
$$ \% \ mathrm {AB} \ \ mathrm {reducción} =\ left [\ left ({\ varepsilon} _ {\ mathrm {ox}} {\ lambda} _2 \ right) \ left (\ mathrm {A} {\ lambda} _1 \ right) - \ left ({\ varepsilon} _ {\ mathrm {ox}} {\ lambda} _1 \ right) \ left (\ mathrm {A} {\ lambda} _2 \ right) / \ izquierda ({\ varepsilon} _ {\ mathrm {rojo}} {\ lambda} _1 \ derecha) \ izquierda ({\ mathrm {A}} ^ {'} {\ lambda} _2 \ derecha) - \ izquierda ({\ varepsilon} _ {\ mathrm {rojo}} {\ lambda} _2 \ right) \ left ({\ mathrm {A}} ^ {'} {\ lambda} _1 \ right) \ right] \ times 100 $$donde, ελ 1 =coeficiente de extinción molar del azul alamar a 570 nm y ελ 2 =el coeficiente de extinción molar del azul alamar a 600 nm, en el oxidado ( ε buey ) y reducido ( ε rojo ) formas. A λ 1 y A λ 2 denotó la absorbancia de los pocillos de prueba.
A ’ λ 1 =absorbancia del pocillo de control negativo a 570 nm.
A ’ λ 2 =absorbancia del pocillo de control negativo a 600 nm.
Ensayo de ALP
La producción de fosfatasa alcalina (ALP) por hMSC cultivada dentro del andamio se midió según el protocolo del fabricante en el kit [12]. Brevemente, se usó PBS estéril (pH 7,4) en el lavado e incubación de armazones, seguido de homogeneización con 1 ml de tampón Tris (1 M, pH 8,0) y sonicación durante 3 min en hielo. Luego se incubaron 25 μL del lisado con 1 mL de solución de p-nitrofenil fosfato (16 mM) a 30 ° C durante 5 min. Se realizaron mediciones espectrofotométricas a 405 nm para monitorear la producción de p-nitrofenol en presencia de ALP.
Actividad de ALP in vivo
Se tomaron nueve ratas desnudas atímicas macho, con un peso de 100 a 120 g cada una, y se disecaron bilateralmente en los músculos abdominales para crear bolsas. Se utilizó un modelo de ratón desnudo para demostrar el potencial osteoinductivo del armazón in vivo. Se cortó uno de cada tres tipos de andamios (5 mm x 5 mm) y se empaquetó en las bolsas de músculos por separado. A continuación, se cerró la bolsa con una sutura no absorbible. Después de 14 días de operación, los implantes se recuperaron extirpando los músculos rectos abdominales y se mantuvieron en PBS. Se escindieron los colgajos musculares y se obtuvo tejido de explante que se homogeneizó en tampón de extracción para liberar fosfatasa alcalina. Se utilizaron 50 μL de alícuota de solución para medir la actividad de ALP.
Análisis estadístico
Todos los experimentos se realizaron por triplicado, y los datos presentados están formateados como media ± desviación estándar (DE) de las muestras, a menos que se mencione. Se realizó un análisis de varianza de una vía (ANOVA) utilizando el software estadístico Origin 6.0, para evaluar las diferencias inciertas y las diferencias significativas. P un valor de 0.05 o menos significa diferencias significativas entre los grupos de estudio.
Resultados
Morfología del andamio
Las imágenes SEM (Fig. 1) del andamio fabricado revelaron una estructura nanofibrosa finamente hilada. Los diámetros promedio de las fibras en los andamios SF y SF + BMP2 parecen ser similares, oscilando entre 100 y 900 nm, en todas las concentraciones, ya que se encuentra que el diámetro es una función del tiempo durante el cual se realizó el electrohilado [13], mientras que el SF Se encontró que las nanofibras eran uniformes y la conjugación de BMP2 condujo a una falta de uniformidad en el diámetro de las fibras. El tamaño de los poros de los armazones parece ser homogéneo en los armazones fabricados y se encuentra que es independiente de la concentración de fibroína. La concentración de SF no afecta significativamente el tamaño de los poros [11].

Micrografías SEM de andamios preparados. un SF. b SF + rhBMP2. c 4SF + rhBMP2
Propiedades mecánicas del andamio
Las curvas de tensión-deformación de los andamios nanofibrosos se representan en la Fig. 2. Se observó que la adición de BMP no altera las propiedades mecánicas del andamio SF, pero con el aumento de la concentración de material de fabricación (SF), se mejoró la propiedad de tracción de las matrices . Puede deberse a la formación de enlaces entre fibras durante la reticulación. Por lo tanto, las fibras SF de baja concentración no exhibieron una mejor resistencia mecánica en comparación con una más alta.
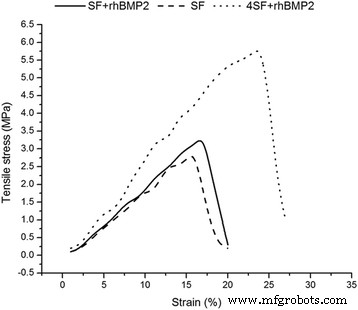
Relación tensión-deformación de las nanofibras electrohiladas. Se comparó la relación tensión-deformación entre (a) SF, (b) SF + rhBMP2 y (c) andamio 4SF + rhBMP2
Estudio de hinchazón
Las relaciones de hinchamiento en función del tiempo para los armazones se representaron en la Fig. 3. Los armazones se hincharon bien con el tiempo de manera uniforme inicialmente y alcanzaron el equilibrio en aproximadamente 380 min. Las fibras unidas a rhBMP2 absorbieron más agua en comparación con los andamios de SF solo, lo que sugiere el aumento de bolsas hidrófilas debido a la asociación de BMP2. Las fibras SF se equilibraron a ∼ 70% mientras que las fibras que contenían BMP2 se equilibraron a ∼ 81% de agua.
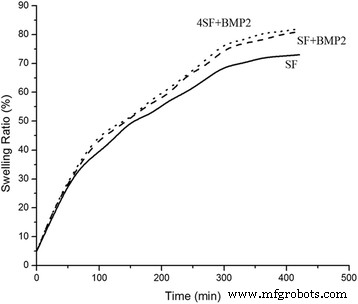
Propiedad de hinchamiento del andamio fabricado. Se observaron cambios en la propiedad de hinchamiento del andamio SF después de la modificación con SF + rhBMP2 y 4SF + rhBMP2
Ensayo de adhesión celular
Se requiere la adherencia de las células al andamio para el crecimiento de las células y la inducción para la diferenciación. En este estudio, observamos que las hMSC se adhirieron bien a los andamios, y la adherencia de las hMSC al andamio 4SF-BMP2, SF-BMP2 y SF se representó en la Fig. 4.
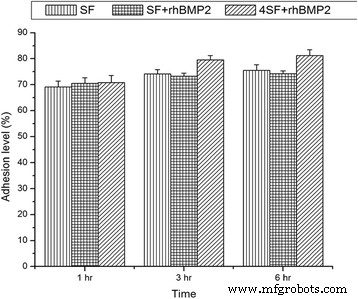
Histograma que representa el porcentaje de adhesión en función del tiempo durante tres momentos. Cambios en el nivel de adhesión en (a) SF, (b) SF + rhBMP2 y (c) andamio 4SF + rhBMP2
Existía preocupación por la pérdida de adherencia en el andamio mixto que se descartó con los resultados observados. La mezcla con BMP2 no disminuye la capacidad de adherencia del andamio. Como es evidente a partir de la Fig. 3, se entendió bien que con un aumento del tamaño de los poros (disminución de la concentración de SF), aumenta la adherencia de la célula al armazón. El ANOVA entre las tres formulaciones diferencia significativamente las variaciones en la tercera y sexta hora. Sin embargo, no se observaron diferencias significativas en la primera hora.
Ensayo de citotoxicidad y ensayo de proliferación celular
La viabilidad celular aumentó significativamente en los armazones conjugados con rhBMP2, y los armazones construidos no crean ningún efecto citotóxico en las células huésped en cuestión (Fig. 4), y las células proliferaron bien en todos los armazones comparativamente. tendencia creciente en la viabilidad con el número de días, y el andamio SF + BMP2 exhibió la menor toxicidad en cada punto de tiempo. ANOVA reveló una diferencia significativa entre los valores de viabilidad celular de las tres formulaciones en cuestión.
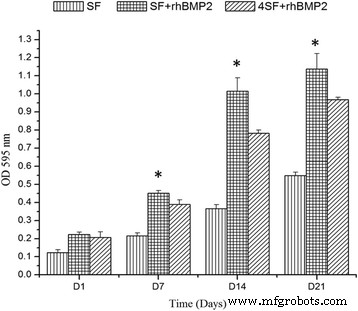
Ensayo de viabilidad celular representado como histograma para cuatro puntos de tiempo. El ensayo de viabilidad celular se realizó mediante ensayo MTT y los resultados se presentan como porcentaje relativo al control
A partir de la Fig. 6, se puede examinar la proliferación celular. Las células proliferaron bien en las tres preparaciones de armazón con mejor en SF + BMP2 en cada punto de tiempo. Los poros más grandes en el andamio SF + BMP2 proporcionaban el espacio máximo para el crecimiento de las células. La importancia de las diferencias entre el grupo quedó bien establecida a partir de ANOVA.
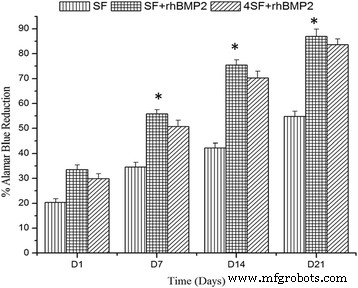
Representación de la proliferación celular como porcentaje de reducción del colorante azul alamar en cuatro puntos de tiempo para SF, SF + BMP2 y 4SF + BMP2
Ensayo de ALP
La actividad ALP es un marcador estándar de la propiedad osteoinductora del entorno alrededor de la célula [13]. En nuestro experimento, observamos una mayor actividad ALP en las construcciones SF + BMP2 en comparación con las construcciones SF solo (Fig. 7). Los andamios nanoestructurados SF también pudieron exhibir osteoinducción sola, pero como es evidente en la Fig. 7 y ANOVA, el andamio SF + BMP2 demostró ser el mejor entre los andamios en cuestión. La concentración de ALP se incrementó a su debido tiempo del experimento, y las construcciones con mayor concentración de SF, sin embargo, exhibieron una menor actividad de ALP en comparación con las construcciones con menor concentración de SF.
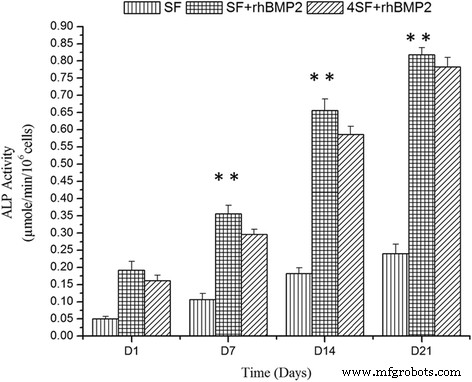
Representación de la actividad ALP entre tres estrategias diferentes de fabricación de andamios en diferentes momentos. (a) SF (b) SF + rhBMP2 (c) 4SF + rhBMP2 andamio
Actividad de ALP in vivo
La Fig. 8 representa la actividad ALP de explantes para (a) SF, (b) SF + rhBMP2 y (c) 4SF + rhBMP2. Como se esperaba, los explantes del tratamiento que contenían rhBMP2 indujeron una mayor actividad de ALP, mientras que los ratones tratados con armazón sin rhBMP2 produjeron una menor actividad de ALP.
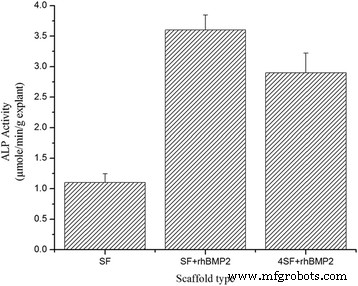
Actividad ALP in vivo de los explantes obtenidos tras el tratamiento. Se utilizó un modelo de ratón desnudo para demostrar el potencial osteoinductivo del andamio in vivo
Discusiones
La ingeniería de tejidos basada en andamios ha demostrado su potencial en la medicina regenerativa y ha sido testigo de un progreso impresionante como herramienta para BTE. Estudios previos han establecido el papel crucial de la microarquitectura y las propiedades físicas de las estructuras en la traducción de construcciones de andamios celulares diseñados in vitro en tejido óseo [14, 15, 16].
Las propiedades mecánicas óptimas (tamaño de poro, resistencia a la tracción, etc.) y la biocompatibilidad de las construcciones son características potenciales a considerar para la colonización y organización celular [17]. El trabajo presentado describe la fabricación y caracterización de andamios para la ingeniería de tejido óseo utilizando una combinación de propiedades beneficiosas de los materiales propuestos para el mismo. Mientras que SF proporciona una plataforma suficientemente fuerte y biocompatible, la rhBMP2 incrustada induce la formación de nuevos osteocitos. SF está siendo estudiado extensamente por varios grupos en diferentes formulaciones para la proliferación de células osteoblásticas [18] y la regeneración de tejidos, incluidos ligamentos, tendones, cartílagos, huesos, hígado, piel, tráquea, córnea, nervios, tímpano y vejiga [19, 20].
Hemos utilizado soluciones acuosas de SF y SF + rBMP2 para nuestro estudio, ya que se prefieren las soluciones acuosas a los disolventes orgánicos para la preparación de soluciones de SF, ya que la degradación de SF es desfavorable en las soluciones orgánicas [18]. Se informó anteriormente que las fibras electrohiladas SF tienen una estructura homogénea de fibras con un diámetro uniforme, y la malla es muy porosa con poros interconectados y entrelazados, lo que también está de acuerdo con nuestro estudio [21, 22]. No hubo ninguna observación de la formación de estructuras en forma de perlas en las fibras SF en nuestros andamios y los informados anteriormente [21]. Se informó anteriormente que el diámetro de la fibra SF pura disminuye con el aumento de la mezcla [11, 21]; sin embargo, no observamos una pérdida de diámetro debido a la mezcla. Pero la uniformidad de la fibra se vio alterada en las fibras mezcladas posiblemente debido a la asociación desigual de rBMP2 en las fibras SF.
Una gran resistencia mecánica es una propiedad esencial para un andamio de tejido. La combinación de SF puro aumentó la flexibilidad de la nanofibra en nuestro experimento, y los informes anteriores también revelaron una tendencia similar en la mejora de las propiedades mecánicas al mezclar SF con otros materiales para producir biomateriales mezclados utilizables [21, 23]. Por lo tanto, nuestro andamio fabricado posee una resistencia mecánica y flexibilidad esenciales que se requieren en aplicaciones de ingeniería de tejidos.
Los andamios para la ingeniería de tejidos deberían poder unir células sobre ellos, deberían facilitar la proliferación celular y la osteoinducción y deberían ser menos citotóxicos para su mejor aceptabilidad. Informes anteriores sobre los andamios SF han establecido sus actividades no citotóxicas y proliferativas de células [21, 24], y nuestros estudios coincidieron estrechamente con los resultados informados anteriormente.
Debido a sus propiedades osteoinductoras, la rhBMP2 está siendo utilizada en la ingeniería de tejidos óseos por varios grupos [25, 26, 27]. Estos estudios han revelado que las células cultivadas sobre armazones que contienen BMP2 poseen una mayor actividad de ALP, un biomarcador de osteoinducción. El efecto de la asociación de BMP2 se contrastó mejor a medida que avanzaba el tiempo de incubación. Kim y col. utilizaron microesferas porosas asociadas a BMP2 y observaron una mejora similar en la osteoinducción [25].
Conclusiones
Fabricamos con éxito andamios fibrosos basados en SF que contienen rhBMP2. Estos andamios eran homogéneos y se encontró que tenían propiedades mecánicas y biocompatibilidad adecuadas. Asociación adicional de rhBMP2 atribuida al potencial osteoinductivo de los andamios fabricados. Los andamios se evaluaron más a fondo para aplicaciones in vivo y se determinó que eran adecuados para aplicaciones que implican ingeniería de tejido óseo.
Abreviaturas
- ALP:
-
Fosfatasa alcalina
- BTE:
-
Ingeniería de tejido óseo
- hMSC:
-
Células madre mesenquimales humanas
- rhBMP2:
-
Proteína 2 morfogénica ósea humana recombinante
- SF:
-
Fibroína de seda
Nanomateriales
- Ingeniería más allá del cubículo
- El CEO de Monroe Engineering es finalista en Emprendedor del año por EY
- El grupo de ingeniería busca llevar la IA de 1 mW al límite
- Diseñando el futuro con robótica
- Principios de ingeniería de confiabilidad para el ingeniero de planta
- Vespel®:El plástico de ingeniería extrema
- Las 3 mejores historias de ingeniería plástica de esta semana
- Los beneficios tangibles de la realidad virtual en el espacio de la ingeniería
- Ingeniería del flujo de luz
- El futuro de la ingeniería de mantenimiento
- Mejore el conocimiento operativo de su empresa



