Oxinitruro de boro y carbono como nuevo fotocatalizador sin metales
Resumen
Los nanomateriales a base de boro están emergiendo como materiales electrocatalizadores (foto) no tóxicos y abundantes en la tierra en la conversión de energía solar para la producción de combustible de hidrógeno solar y la remediación ambiental. El oxinitruro de boro y carbono (BCNO) es un semiconductor cuaternario con propiedades electrónicas, ópticas y fisicoquímicas que se pueden ajustar variando la composición de boro, nitrógeno, carbono y oxígeno. Sin embargo, la relación entre la estructura de BCNO y la relación de actividad fotocatalítica aún no se ha explorado. Realizamos un análisis espectroscópico en profundidad para dilucidar el efecto del uso de dos precursores de nitrógeno diferentes y el efecto de las temperaturas de recocido en la preparación de BCNO. Nanodiscos BCNO ( D =6,7 ± 1,1 nm) con patrones de difracción de nitruro de boro turboestrático se prepararon usando clorhidrato de guanidina como precursor de la fuente de nitrógeno tras el recocido térmico a 800 ° C. El análisis elemental de superficie de espectroscopía de fotoelectrones de rayos X (XPS) de los nanodiscos de BCNO reveló que las composiciones de B, C, N y O eran del 40,6%, 7,95%, 37,7% y 13,8%, respectivamente. Según el estado sólido 11 Los análisis de RMN B, los nanodiscos de BCNO derivados del clorhidrato de guanidina mostraron la formación de varios BN tricoordinados x (OH) 3− x especie, que también sirvió como uno de los sitios activos fotocatalíticos. La XRD y los análisis espectroscópicos en profundidad corroboraron la preparación de nanodiscos hexagonales de nitruro de boro dopados con BCNO. Por el contrario, el BCNO recocido a 600 ° C utilizando melamina como precursor de nitrógeno consistió en nanohojas en capas compuestas por átomos de B, C, N y O unidos covalentemente en una red de panal como evidencia de XRD, XPS y NMR de estado sólido análisis ( 11 B y 13 C) análisis. La composición elemental de la superficie de XPS de las estructuras en capas de BCNO derivadas de melamina consistía en una composición de alto contenido de carbono (75,1%) con una composición relativamente baja de boro (5,24%) y nitrógeno (7,27%), lo que indicaba la formación de óxidos de grafeno dopados con BCNO. Estructuras de láminas en capas. Se descubrió que esta serie de estructuras en capas de óxido de grafeno dopado con BCNO derivadas de melamina exhiben la actividad fotocatalítica más alta, superando la actividad fotocatalítica del nitruro de carbono grafítico. En esta estructura en capas, la formación del tetracoordinado BN x (OH) 3− x Se propuso que las especies (CO) y los dominios grafíticos ricos desempeñaran un papel importante en la actividad fotocatalítica de las estructuras en capas de óxidos de grafeno dopados con BCNO. Se midió que las energías de banda prohibida óptica eran de 5,7 eV y 4,2 eV para nanodiscos de nitruro de boro hexagonales dopados con BCNO y estructuras en capas de óxidos de grafeno dopados con BCNO, respectivamente. Finalmente, BCNO exhibió una fotoluminiscencia ultralarga con una vida media de desintegración de 1,58, 2,10, 5,18 y 8,14 µs para BGH01, BGH03, BMH01, BMH03, respectivamente. Este estudio proporciona un nuevo sistema fotocatalítico libre de metales y proporciona el primer análisis estructural con respecto al origen del fotocatalizador basado en BCNO.
Resumen gráfico
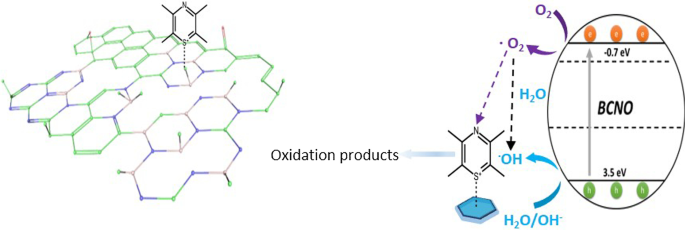
Introducción
Los nanomateriales sin metales están emergiendo como catalizadores (foto) ecológicos y rentables con altas estabilidades estructurales y químicas para diversas aplicaciones, incluida la producción de combustible solar, la remediación ambiental, CO 2 reducción, desinfección de microorganismos nocivos y síntesis química selectiva de compuestos orgánicos [1, 2, 3, 4, 5, 6, 7]. En comparación con sus contrapartes de metal, un catalizador sin metal también es menos propenso a envenenamiento y conduce a ciclos de vida más largos. Por lo tanto, la búsqueda y el desarrollo de nuevos materiales que sean fotocatalizadores estables, eficientes y rentables siguen siendo esfuerzos de investigación críticos y desafiantes. Los materiales a base de carbono, como el nitruro de carbono grafítico (CN) [4, 8, 9], el punto de carbono (C-dot) [2, 3, 10] y los materiales a base de grafeno [7, 11] se han investigado ampliamente. debido a sus excelentes propiedades fisicoquímicas, estabilidades estructurales y químicas, y la facilidad de síntesis a partir de elementos abundantes en la tierra. Recientemente, se han desarrollado (foto) catalizadores a base de boro como sistemas fotocatalíticos sin metales con un rendimiento notable. En particular, el carburo de boro, conocido por su dureza, mostró generación de hidrógeno fotocatalítico de luz visible libre de metales, superando al fotocatalizador CN basado en carbono de última generación [12, 13]. Nanohojas de nitruro de boro (BCN) hexagonal dopado con carbono de gran área superficial que exhiben actividad fotocatalítica de luz visible para H 2 y O 2 generación así como CO 2 la reducción y la captura han dado lugar a nuevas posibilidades en el fotosistema [14, 15]. Otro (foto) electrocatalizador que contiene boro, como oxinitruro de boro (BNO) [16, 17], fosfuro de boro (BP) [18, 19], grafeno dopado con boro [20], nitruro de carbono boro (BCN) [14], nitruro de carbono dopado con boro ( CN dopado con B ) [21] y el boro elemental [22, 23] han demostrado actividades (foto) electrocatalíticas significativas [13].
El oxinitruro de boro y carbono (BCNO) es un nanomaterial a base de boro que se ha estudiado menos que otros materiales. Fue desarrollado por primera vez después de su predecesor BCN, un semiconductor con una banda prohibida de aproximadamente 2 eV, para reemplazar fósforos tóxicos basados en compuestos de oxinitruro y nitruro [24, 25]. La sustitución de los átomos de B, C, O y N en la red de grafeno o nitruro de boro hexagonal (hBN) dio lugar a compuestos de BCNO con propiedades de fotoluminiscencia sintonizables y una banda prohibida que oscilaba entre 0 eV (grafeno) y 5,9 eV (hBN) [26]. . Estas deseables propiedades de semiconducción y fotoluminiscencia han atraído recientemente a investigadores para desarrollar una nueva metodología sintética para sintetizar nanoestructuras de BCNO de baja dimensión con mayor cristalinidad [27], formas controladas [28] y estructuras 2D atómicamente delgadas [29]. Trabajos anteriores investigaron los efectos de las temperaturas y los tiempos de recocido en la modulación de la propiedad de fotoluminiscencia de BCNO sin proporcionar una caracterización estructural en profundidad [30, 31]. En este artículo, investigamos el efecto del uso de diferentes precursores de fuentes de nitrógeno, temperaturas de calcinación (800 ° C frente a 600 ° C) y tiempos de calcinación (0,5 h frente a 12 h) sobre la actividad fotocatalítica de estructura de nanoestructuras de BCNO.
Métodos
Productos químicos e instrumentos
Ácido bórico 99,99% (H 3 BO 3 ), melamina 99% (C 3 H 6 N 6 ) y hexametilentetramina ≥ 99% (C 6 H 12 N 4 ) se adquirieron de Alfa Aesar y se utilizaron sin purificación adicional. Clorhidrato de guanidina al 99,5% (CH 5 N 3 HCl) se adquirió de Arcos Organics. BCNO se sintetizó de acuerdo con la literatura mediante el método de recocido a baja temperatura [25, 32]. El análisis de UPS se realizó en un ULVAC-PHI PHI 5000 Versaprobe II usando He I 21.22 eV como fuente de fotones con polarización de 5 V. La morfología de las muestras de BCNO se analizó mediante un microscopio electrónico de transmisión (JEOL, JEM-ARM200FTH). Las difracciones XRD se obtuvieron usando el espectrómetro Bruker D2. Los espectros de emisión de fotoluminiscencia en solución se obtuvieron utilizando un espectrómetro de fotoluminiscencia (PerkinElmer, LS55) y los espectros de absorción óptica de BCNO en solución se determinaron mediante el espectrómetro UV-Vis (HITACHI, U-3900). La espectroscopia de fotoelectrones de rayos X se analizó mediante un espectrómetro de fotoelectrones de rayos X de alta resolución (ULVAC-PHI, PHI Quantera II) utilizando rayos X de Al Ka como fuente de excitación. La solución de BCNO se vertió gota a gota sobre el sustrato de silicio para la caracterización de XPS. La energía de enlace se calibró en carbono a 284,8 eV. La deconvolución y el ajuste de picos de XPS se realizaron utilizando el software CACS XPS. La PLQY absoluta se realizó de acuerdo con la bibliografía [33] y se detectó mediante una cámara CCD (PIXIS 256BR, Princeton Instruments). La medición del PLQY absoluto se realizó mediante el uso de un espectrógrafo de fibra, incluido un sistema de esfera integradora calibrada (Labsphere) y una cámara de dispositivo de carga acoplada (CCD) (PIXIS 256BR, Princeton Instruments). Un láser de diodo ( λ =375 nm, Becker &Hickl GmbH) como fuente de bombeo. La fotoluminiscencia resuelta en el tiempo se midió en una configuración frontal utilizando un láser de nitrógeno pulsado ( λ =337,1 nm, LTB Lasertechnik Berlin GmbH) como fuente de excitación, que fue activada por un generador de retardo digital (DG645, Stanford Research Systems). Las señales se detectaron mediante un tubo fotomultiplicador de conteo de fotones (PMC-100-1, Becker &Hickl GmbH), y los recuentos de fotones se acumularon con un módulo multiescaler (MSA-300, Becker &Hickl GmbH). Los espectros de infrarrojos se registraron mediante un espectrómetro de infrarrojos de transformada de Fourier (Bruker, Vertex 80v) utilizando reflectancia total atenuada (ATR). Los espectros de resonancia magnética nuclear se obtuvieron usando un espectrómetro de RMN Bruker Avance III 400 equipado con un imán de 9,4 T usando una sonda de giro de ángulo mágico (MAS) de 4 mm. 11 Las RMN B MAS se registraron utilizando el método de eco de espín con una velocidad de giro de 10 kHz. Se recogieron 8000 exploraciones con un retardo de reciclado de 4 s. Los desplazamientos químicos se hicieron referencia a 1 M H 3 BO 3 solución acuosa a 19,6 ppm. 13 Los espectros C CP / MAS NMR se registraron usando una secuencia de polarización cruzada (CP) con una velocidad de giro de 12,5 kHz. Se recogieron 30.000 exploraciones con un retraso de reciclaje de 4 s. Todos los 13 C se hizo referencia a los desplazamientos químicos al trimetilsilano puro utilizando la referencia secundaria del adamantano CH 2 pico a 38,48 ppm.
Preparación de BCNO
En este estudio, se prepararon dos series de BCNO utilizando dos fuentes precursoras de nitrógeno diferentes mientras se fijaban las fuentes precursoras de boro y carbono, las proporciones de precursores, la temperatura de recocido y el tiempo. El efecto de las temperaturas y los tiempos de recocido también se investigó fijando todos los demás parámetros de reacción para cada serie de BCNO preparada en este estudio. Brevemente, los tres componentes precursores en una proporción molar predeterminada se agregaron a agua destilada y se calentaron a 90 ° C hasta que la solución pareció homogénea (Tabla 1). La mezcla glutinosa se secó en un horno durante la noche, produciendo un sólido blanco seco. El sólido blanco se molió con un mortero y una mano hasta obtener polvos finos. El precursor sólido se calcinó en el horno a una temperatura y un tiempo predeterminados, como se muestra en la Tabla 1, con una velocidad de rampa de 5ºC / min a presión atmosférica ambiente. La muestra de polvo teñida de amarillento se molió hasta obtener un polvo fino después de que el horno se enfrió naturalmente a temperatura ambiente.
Estrategias de purificación de BCNO
El BCNO preparado se purificó mediante centrifugación a 6000 rpm durante 10 min en agua y etanol (1:10 v / v en una concentración de 10 mg / ml). Después de la centrifugación, el producto se redisolvió en agua destilada, se diluyó con etanol en una relación 1:10 v / v de agua:etanol. El BCNO purificado se depositó sobre una rejilla de cobre recubierta de carbono para el análisis TEM. Para la preparación de muestras de SEM y XPS, la muestra de BCNO purificada se vertió gota a gota sobre una oblea de silicio. Antes de la deposición de la muestra, las obleas de silicio se limpiaron mediante sonicación con agua, propanol y acetona durante 10 minutos en cada disolvente. La muestra de UPS se preparó de manera similar al procedimiento descrito para las muestras de SEM y XPS, excepto que las muestras se depositaron sobre un vidrio recubierto de óxido de indio y estaño (ITO).
Preparación de nitruro de carbono (CN) a granel
El CN a granel se sintetizó mediante un método sencillo descrito en la bibliografía [34]. Brevemente, se colocó polvo de melamina en un crisol y se recoció a 550 ℃ durante cuatro horas con una velocidad de aumento de 5 ℃ / min a presión atmosférica ambiente.
Procedimiento de degradación del tinte fotocatalítico
Las actividades fotocatalíticas de varias muestras de BCNO se evaluaron mediante la fotodegradación con azul de metileno (MB) como reacción modelo. En un experimento típico de degradación del tinte, se agregaron 10 mg de muestra de BCNO a un vial de muestra que contenía 15 ml de solución de MB (10 ppm). Después de agitar durante 10 min en la oscuridad, el vial de muestra se irradió con una lámpara de xenón de 100 W (250 nm ~ 1100 nm). Las muestras cinéticas (2 mL) se extrajeron usando una pipeta de la solución en un intervalo de tiempo de 20 min hasta que el tiempo total de degradación fotocatalítica alcanzó los 80 min. Se analizaron muestras cinéticas a diferentes intervalos de tiempo mediante un espectrómetro UV-vis. El cambio en la concentración de metilbromuro se obtuvo mediante la ley de Beer.
Resultados y discusión
Síntesis de BCNO
En nuestra investigación para la preparación de nanoestructuras de BCNO de baja dimensión con alta cristalinidad para facilitar el transporte de carga, descubrimos BCNO con estructuras químicas y actividades fotocatalíticas claramente diferentes. Basándonos en la síntesis de BCNO reportada en la literatura [25, 32], investigamos el efecto del uso de dos fuentes diferentes de precursores de nitrógeno, así como el efecto de las temperaturas de recocido térmico y el tiempo en la evolución de la estructura-propiedad de BCNO. En este estudio, se prepararon dos series de BCNO utilizando ácido bórico y hexametilentetramina como fuentes de boro y carbono, respectivamente (Tabla 1). El BCNO se sintetizó utilizando melamina y clorhidrato de guanidina como fuente de nitrógeno y se indica como BMH y BGH, respectivamente. Después de investigar sistemáticamente cada condición de reacción, la serie BMH solo exhibió actividades fotocatalíticas cuando se recoció a la temperatura más baja de 600 ° C durante 12 h. La serie BGH solo exhibió actividades fotocatalíticas con recocido a alta temperatura a 800 ° C durante 12 h. En ambas series, las relaciones molares de ácido bórico, melamina y clorhidrato de guanidina se fijaron en 3:1, mientras que las relaciones molares de hexametilentetramina se variaron de 0,1 a 0,3. Estas proporciones del precursor de hexametilentetramina se indican en los nombres de las muestras como BMHH01 / BGH01 y BMH03 / BGH03, respectivamente (Tabla 1).
La Figura 1 muestra las imágenes TEM representativas de BGH calcinadas a 800 ° C durante 12 h compuestas por un núcleo cristalino con morfología de nanopartículas cuasi esféricas y D =6,7 ± 1 nm. La BGH preparada se dispersó fácilmente en agua (archivo adicional 1:Fig. S1), y como lo demuestra la deposición de nanopartículas discretas en la rejilla de cobre TEM. La dispersabilidad acuosa de BGH y BMH se origina muy probablemente a partir de la estabilización electrostática basada en su potencial de superficie cargado negativamente de BGH y BMH. De estado sólido 11 Los análisis de RMN B revelaron que la abundancia de grupos hidroxilo en las nanoestructuras de BMH y BGH corroboró su capacidad de dispersión en medios acuosos. Con gran aumento, cada nanopartícula cuasi esférica exhibió un espaciado de celosía distintivo de los planos (002) medidos en 0.338 nm, lo que es consistente con los informes de la literatura [24, 35] (Fig. 1c). En comparación con la nanopartícula de BCNO de 5 nm obtenida mediante recocido térmico en el ambiente de sal eutéctica, las nanopartículas de BGH preparadas en este trabajo poseían una alta cristalinidad [25] (Fig. 1). A continuación, caracterizamos BMH que se preparó en base a un informe de la literatura utilizando ácido bórico, melamina y hexametilentetramina y se recoció a 600 ° C durante 12 h. En contraste con la morfología de BGH, BMH se compone de láminas de varias capas con formas mal definidas (Fig. 1). A mayor aumento, la imagen TEM de los bordes en las láminas multicapa (Fig. 1d) reveló nano láminas con características de distorsión estructural [36] como se muestra en la Fig. 1e. La Figura 1f muestra una imagen SEM representativa del BMH que incluye agregados de tamaño micrónico sin rasgos distintivos. Sin embargo, a diferencia de la serie BGH, la calcinación a una temperatura más alta a 800 ° C usando melamina como precursor de la fuente de nitrógeno no produjo una morfología de nanodisco. El TEM, XRD, la absorbancia UV y la fotoluminiscencia de los otros compuestos de las series BGH y BMH sintetizados en diferentes condiciones de reacción están disponibles en ESI.

Micrografía electrónica de transmisión (TEM) y micrografía electrónica de barrido (SEM) representativas de la BGH y la BMH preparadas depositadas a partir de una solución de etanol diluida. un , b TEM de aumento alto y bajo de BGH, c TEM de alta resolución de BGH con un espaciado de celosía distinto (002) de 0.338 nm, d Imagen TEM de BMH representativa a bajo aumento, e Imagen TEM ampliada del área encuadrada en la Fig.1 d mostrando características de distorsión estructural dentro del óxido de grafeno en capas, y f imagen SEM representativa de BMH
La Figura 2 muestra los patrones XRD de BMH03 (traza verde), BMH01 (traza roja) y BGH01 (traza azul) preparados en nuestro laboratorio en las condiciones de reacción prescritas que se enumeran en la Tabla 1. El BGH01 exhibió picos de difracción amplios centrados alrededor de 26.6 ° y 43,1 ° (2θ), que es el patrón de difracción característico del nitruro de boro turboestrático (t-BN). El pico ancho centrado alrededor de 26,6 ° se originó en el plano de reflexión (002), y el pico ancho de 43,1 ° corresponde al plano de reflexión (10) inducido por nitruro de boro hexagonal (h-BN) [37]. El patrón XRD de BMH estuvo dominado por dos patrones de difracción amplios a 2θ de aproximadamente 25.4 ° y 42.4 °, que son patrones de firma para las bandas (002) y (10), respectivamente, de la estructura cristalina hexagonal del grafito [38]. La banda comúnmente denotada (10) también está asociada con la reflexión 2D del carbono turboestrático [39]. Además, la ausencia de un pico en 2θ alrededor de 10,9 ° y la aparición de una banda ancha alrededor de 25,4 ° se debió a la incorporación de dopantes o impurezas dentro de la estructura del grafeno o los óxidos de grafito [40,41,42,43, 44,45]. Por lo tanto, es razonable proponer que la estructura dominante de BMH son óxidos de grafeno dopados.
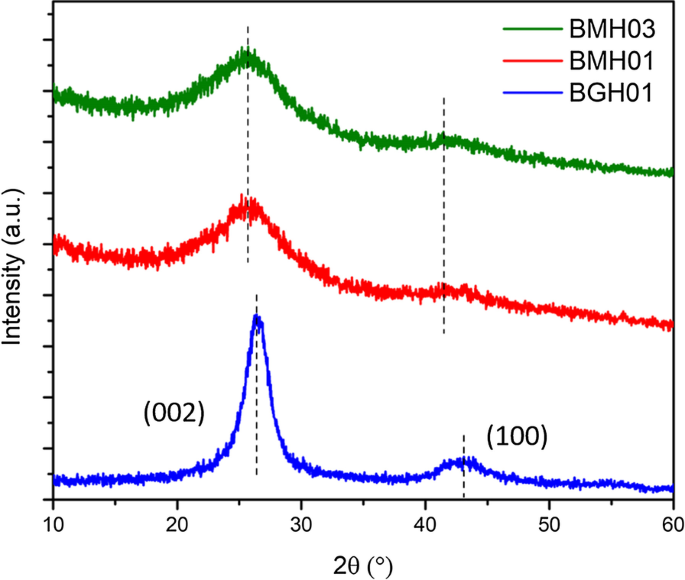
Los patrones XRD de policristalinos BMH03 (trazo verde), BMH01 (trazo rojo), BGH01 (trazo azul) y BGH01. El pico ancho de la serie BGH01 en ca. 26,6 ° representa la reflexión del plano (002) de h-BN y otro pico ancho en ca. 43,1 ° representa los planos de reflexión no resueltos de h-BN. Los patrones de difracción del BMH mostraron dos amplias reflexiones centradas en alrededor de ~ 25,4 ° y ~ 42,4 °. Los patrones XRD de otras series de BCNO se muestran en el archivo adicional 1:Figura S3)
Análisis estructural de BGH (serie guanidina)
La espectroscopía XPS, FTIR y RMN de estado sólido se realizaron para producir una comprensión más profunda de la estructura molecular de BGH. El XPS se utilizó para confirmar la presencia de los electrones a nivel del núcleo de los elementos B, C, N y O y sus respectivos enlaces químicos en los compuestos BGH. Las figuras 3a-e muestran un espectro XPS típico de los nanodiscos de BGH. De acuerdo con los análisis de composición elemental de superficie de XPS, BGH contenía un alto contenido de B y N (aproximadamente 40% cada uno), con una menor composición de C y O de aproximadamente 8% y 13%, respectivamente (Archivo adicional 1:Tabla S3). La estequiometría cercana a 1:1 de la composición de B y N es acorde con los análisis de XRD, que confirmaron que la BGH01 preparada en nuestro laboratorio estaba compuesta por una estructura de nitruro de boro turboestrático. Todos los espectros XPS se ajustaron con una función gaussiana con R 2 > 0,99, que está representado por las curvas roja y verde en los espectros XPS para cada elemento. Para la serie BGH, los B 1 los espectros se deconvolucionaron en dos curvas ajustadas, que correspondían al enlace B-O (a una energía de enlace de 189,7 eV) y al enlace B-N (a una energía de enlace de 190,7 eV). Los N 1 los espectros se ajustaron con dos curvas gaussianas compuestas de enlace N-B con 397,3 eV de energía de enlace y enlace B-N – O con 398 eV de energía de enlace [46]. Los enlaces N-B y B-N-O indicaron la presencia de hBN dopado con O o la formación de un compuesto de BNO [47]. Dado que la síntesis de BGH se realizó en condiciones atmosféricas, también se incorporó un átomo de oxígeno en el dominio h-BN para la unión B-O, como se informa en la literatura [47]. Esta hipótesis se confirmó analizando los O 1s espectros, que mostraron un solo pico correspondiente al enlace B-O (energía de enlace a 532 eV). Este resultado apoya aún más nuestra hipótesis inicial de que la serie BGH está compuesta de hBN dopado con O, y la mayoría del átomo de oxígeno está unido al átomo de boro. Los C 1 del espectro de BGH se deconvolucionó en tres especies C, a saber, C-O, C-B y C-O-C, que se unieron a 283,7 eV, 285 eV y 287 eV, respectivamente. Debido a la baja composición de C y una estequiometría 1:1 de B y N en la serie BGH, especulamos además que la estructura de BGH01 es h-BN dopada con C y O. La estructura propuesta fue apoyada por la formación de enlaces C-B, B-O y B-N-O dentro del dominio hBN, como se evidencia en los espectros XPS (Fig. 3). Por tanto, es razonable deducir la estructura de los nanodiscos de BGH preparados a 800 ° C como C y hBN dopado con O. Además, la XRD en polvo y la TEM de alta resolución apoyaron la formación de B, C, N y O unidos covalentemente en una red en forma de panal con un espaciado de red similar al del nitruro de boro turboestrático. A lo largo de este manuscrito, la estructura de BGH01 se denominará hBN dopado con BCNO.
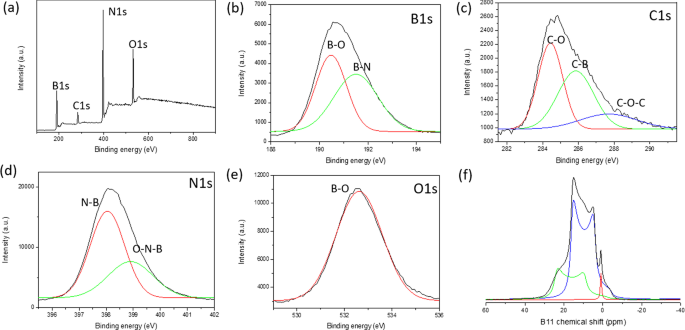
un Espectros de levantamiento XPS de BGH01. Espectros de nivel central de b B 1s , c C 1s , d N 1s y e O 1s . Cada pico deconvolucionado está equipado con funciones gaussianas. f El 11 B espectros de RMN MAS de estado sólido de BGH01. ( 11 B MAS NMR de estado sólido de BGH01-LT se muestra en el archivo adicional 1:Figura S10)
También investigamos el efecto de las temperaturas y los tiempos de calcinación sobre la actividad fotocatalítica estructura de las nanoestructuras de BCNO mientras se mantienen constantes los demás parámetros de síntesis. Al aumentar la temperatura de reacción (de 600 ° C a 800 ° C) y aumentar los tiempos de reacción de 30 minutos a 12 horas, hubo un aumento general en la unión B-N y B-O (archivo adicional 1:Figura S6). Por el contrario, la unión B-C disminuye con el aumento de la temperatura y el tiempo de reacción, lo que implica la formación de enlaces B-N y B-O hexagonales energéticamente estables mientras se sacrifican los enlaces B-C metaestables [48]. Como se anticipó, la composición de enlace B-C aumenta al aumentar la proporción de precursor de hexametilentetramina (como fuente de C) mientras se mantienen constantes los otros parámetros [49]. En el ESI se proporciona una tendencia más detallada de la evolución de enlaces químicos de BGH preparada a diferentes temperaturas, tiempos y proporciones de precursores de calcinación (archivo adicional 1:Figura. S6 y S7).
1 El 11 Se utilizó MAS NMR de estado sólido B para analizar cuantitativamente cada composición de enlace relacionada con B en BGH y BMH cuantitativamente. A continuación, presentamos la primera caracterización estructural detallada de BCNO a nivel molecular utilizando MAS en estado sólido 13 C y 11 B NMR para reunir enlaces específicos relacionados con C y B. Aunque los nanomateriales de hBN y sus propiedades electrónicas inducidas por defectos han atraído un interés significativo, la estructura molecular de los bordes y la estructura de los defectos de hBN son en gran parte desconocidas [50]. La falta de caracterización estructural de los nanomateriales relacionados con el boro se debe a la dificultad de analizar el estado sólido 11 Espectro de RMN B porque 11 B es un núcleo cuadrupolo medio entero ( I =3/2) [51, 52]. De estado sólido 11 La RMN B también es difícil de interpretar debido al acoplamiento cuadrupolo de segundo orden que da como resultado la distorsión de la señal, que solo puede promediarse parcialmente mediante MAS RMN [53]. Además, el rango de desplazamiento químico para 11 La RMN B es relativamente estrecha, lo que hace que la asignación de picos anchos, superpuestos y distorsionados de varias especies de boro sea extremadamente desafiante [54]. En este estudio, realizamos 11 B RMN de estado sólido registrada a 9,4 T, y el espectro se deconvolucionó usando análisis en forma de línea sólida de efecto de giro superior (SOLA). Siguiendo el CP-MAS 11 En el experimento de RMN B informado en la literatura, obtuvimos información significativa de enlaces químicos relacionados con B al tener en cuenta la constante de acoplamiento cuadrupolar ( C Q ) y la asimetría del tensor del gradiente de campo eléctrico (EFG) ( η Q ) [51, 52, 55]. La Figura 3f muestra el estado sólido 11 Espectros de RMN de eco de espín B de BGH con tres picos principales y δ iso centrado en 28,3 ppm, 20 ppm y 1,2 ppm, respectivamente. Basado en estudios de literatura sobre CP-MAS 11 B NMR de nitruro de boro y sus estructuras relacionadas, el pico con un δ iso de 28,3 ppm (ajuste de traza verde) y una C Q de 2,85 MHz correspondió al BN 2 trigonal-planar (OH) especies con un solo grupo hidroxilo [53,54,55]. Cuando el grupo hidroxilo o el átomo de puente de oxígeno reemplazó al átomo de nitrógeno alrededor de los sitios de boro trigonal-planar, una nueva especie B con un δ iso aparecieron 20 ppm (ajuste de traza azul). Esta señal de cambio químico más baja probablemente se atribuyó a otro sitio de boro trigonal con dos grupos hidroxilo o un grupo hidroxilo y un átomo de oxígeno puente (BN (OH) 2 o sitios BNO (OH)). El pico agudo en δ iso de 1,2 ppm (ajuste de trazo rojo) corresponde a un sitio B tetraédrico de cuatro coordenadas, probablemente coordinado por nitrógeno y múltiples grupos hidroxilo o un átomo de oxígeno puente (52-54) o enlaces C-B relacionados con el carbono [46, 52]. El CP-MAS 11 El análisis de B NMR de BGH01 reveló varios enlaces B-N, O-B y B-C acordes con los análisis XPS y XRD. Además, el estado sólido 11 B NMR también reveló que la mayor parte del boro estaba unido con nitrógeno y con uno o más grupos hidroxilo como BN x (OH) 3− x especies. Se especuló que estas especies hidroxiladas proporcionarían estabilidad coloidal en la solución acuosa mediante enlaces de hidrógeno y estabilización electrostática. También observamos una reducción en las especies B tetracoordinadas como BN x (OH) 4− x o BN x (O) (OH) 3− x (en el que O es el oxígeno puente) y los anillos de boroxol [54, 56] con una temperatura de reacción en aumento. Al mismo tiempo, varios BN tricoordinados x (OH) 3− x especies surgieron cuando la temperatura de recocido aumentó de 600 ° C a 800 ° C (archivo adicional 1:Figura S8 y S10). Este resultado implicó que a altas temperaturas, el anillo de boroxol reaccionaba con amoníaco para formar varios BN x hidroxilados. (OH) 3− x o BN x (O) (OH) 2− x especie [55] (Archivo adicional 1:Fig. S10).
Análisis estructural de BMH
Basado en nuestro riguroso análisis estructural a través de XPS y FTIR, así como 11 B y 13 C MAS NMR en estado sólido, se propuso que la estructura de BMH fuera óxidos de grafeno dopados con BCNO. De acuerdo con el análisis elemental de superficie de XPS, BMH estaba compuesto por un 75% de especies de carbono y solo un 5% de especies relacionadas con el boro (Archivo adicional 1:Tabla S3). Los B 1 desconvolucionados los espectros mostraron enlaces BCN y BN a energías de enlace de 191,7 y 192,4 eV, respectivamente (Fig. 4). Los C 1 especies mostraron dos señales de fotoemisión distintas, que correspondían a la unión C – C (sp 2 y sp 3 Enlace C-C) con una energía de enlace de aproximadamente 285,0 eV, y un componente más débil surgió del enlace B-C-N que aparece en 285,6 eV [57]. Las otras señales relativamente pequeñas a 288.0 eV y 288.7 eV se debieron a C-N 3 y enlace C =O, respectivamente [46, 57, 58]. Se especuló que el átomo de C oxigenado (C =O) se formaría en los bordes de los dominios de óxido de grafeno, y el C-N 3 la unión fue el pico característico de la CN. Los N 1 Los espectros XPS, centrados en 399,0 eV de energía de enlace, se pueden ajustar con dos curvas gaussianas compuestas de C-N-B a 399,2 eV de enlace y C =N de enlace a 400,0 eV [46, 57, 59, 60]. Según el análisis de XPS, la serie BMH comprendía solo entre el 10 y el 25% de la unión relacionada con O en comparación con aproximadamente el 35% de la unión relacionada con O en la serie BGH. Los O 1 los espectros centrados en 531,2 eV de energía de enlace se pueden descomponer en enlaces C =O y CO, lo que podría atribuirse al dominio de óxidos de grafeno. Los 13 C CP-MAS NMR de estado sólido mostró además la presencia de unión grafítica C =C a 40,2 ppm, lo que corrobora con los resultados de XRD y XPS [38] (Fig. 5). En cada una de las series de BMH informadas en este documento, las 13 La C NMR mostró dos proporciones equimolares de especies de carbono a 160 y 154 ppm correspondientes a C α y C β , respectivamente, que se encuentra típicamente en estructuras de nitruro de carbono grafítico [61] (Fig. 5 y Archivo adicional 1:Tabla S4). Compared to the bulk CN synthesized according to the literature procedure [34], the chemical shift of the signature resonance for C α and C β peak appeared at 164 and 156 ppm, respectively (Fig. S13). Boron doping into the CN heptazine structure could have contributed to these slight chemical shift differences between the BMH series and the bulk CN (Additional file 1:Fig. S13).
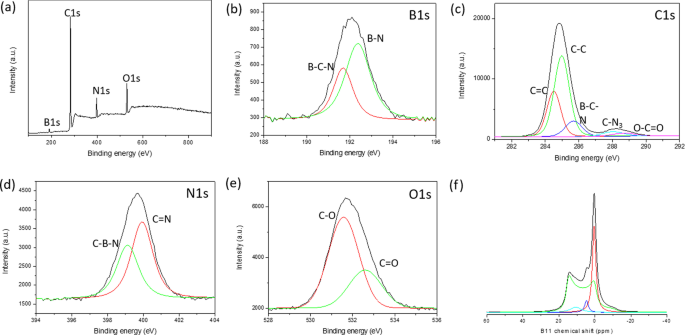
a Survey XPS spectra of BMH01 and 11 B NMR spectra. Core level spectra of b B1s , c C1s , d N1s , and e O1s . Each core spectra were fitted with a black trace, while the red and green traces under the peak were deconvoluted using a Gaussian function. f 11 B solid-state MAS NMR were deconvoluted using SOLA analysis to tricoordinate and tetracoordinate B-sites. The XPS and 11 B solid-state MAS NMR of other BMH series compounds can be found in Additional file 1:Figure S7, S11, and S12)
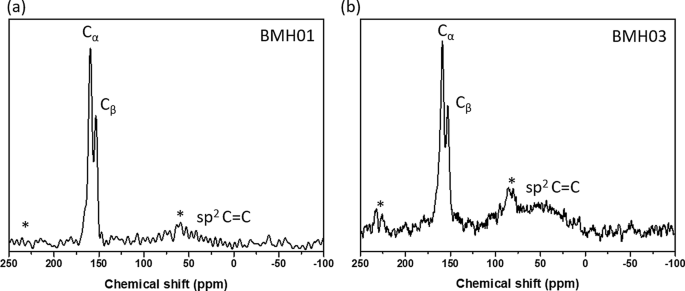
Solid-state 13 C MAS NMR of a BMH01 and b BMH03
Due to the abundant evidence of the presence of carbon nitride (CN) in the BMH series based on solid-state NMR spectroscopy (Fig. 5), we considered three possibilities of interactions between BCNO-doped graphene oxide and CN in BMH, namely:(i) bulk phase separation, (ii) disordered 2D network, and (iii) layered intercalation [62]. To eliminate the possibility of bulk phase separation, we examined the XRD pattern of CN nitride andBMH as well as a physical mixture of both in a 1:1 mass ratio. We found that the XRD patterns of the mixtures showed only the diffraction pattern of the bulk CN with a slight reduction in the crystallinity compared to the pristine CN diffraction [63] (Additional file 1:Fig S4). Since the XRD pattern of BMH did not possess any diffraction peaks that corresponded to CN, this experimental result confirmed that CN did not form as a bulk-separated domain during the synthesis of BMH (Additional file 1:Fig. S4). We also considered the formation of a disordered 2D network, in which CN and the doped-graphene oxides are bonded on the same 2D plane [62]. Based on a literature report on a CN/graphene oxide 2D matrix, the XRD pattern of a disordered 2D network showed characteristic peaks for both species with a slight peak broadening and a slight peak shifting [64]. However, the XRD pattern of BMH (Fig. 2) did not contain any signature diffractions of CN. A previous study also showed that characteristic peaks of graphene oxide disappeared in a graphitic CN/amorphous CN/graphene oxide composite due to the layer-by-layer interactions [65]. Therefore, it is reasonable to propose that CN is intercalated between the doped-graphene oxide layers. The FTIR spectrum of the selected BGH and BMH series is shown in Additional file 1:Fig. S5.
Boron-related bonding within the BMH series was investigated using 11 B solid-state MAS NMR at 9.4T, and the broad NMR spectrum was deconvoluted using the SOLA analysis showing the presence of both tricoordinate and tetracoordinate boron site. The SOLA analysis yielded four line fittings under the broad 11 B NMR spectrum, which could be assigned as trigonal planar BN2 (OH) or BN2 O at a δiso of 19.8 ppm and a CQ of 2.85 MHz (green fitting). The bay and corner B sites as in B-doped CN appeared at a δ iso of 5 ppm and δ iso of 11 ppm, respectively [61]. These assignments are also commensurate with the formation of CN based on the 13 C NMR and XPS analyses. Compared to the BGH series, the relative composition of the tetracoordinate B(IV) site of BMH was much higher (ca. 55% in the BMH series vs. 3% in the BGH series). However, the tetracoordinate B(IV) species in BMH appeared at a lower chemical shift than those found in BGH (Fig. 3f) and was therefore presumed to be the BN2 (OC)2−x (OH)x species [46]. Notably, the h-BN domain was absent from the BMH series prepared via thermal annealing at a lower temperature (600 °C). However, upon increasing the thermal annealing temperature from 600 °C to 800 °C, the structures of BMH01HT-30 min and BMH01HT-12 h showed a high composition of tetracoordinate BN2 (OH)2 species and the tricoordinate BN3 bonding (Additional file 1:Fig. S11 and S12). The presence of a high composition of tetracoordinate BN2 (OH)2 and BN3 bonding was shared among all the inactive BCNO investigated in this study. Moreover, although BMH01HT-12 h possessed an identical surface elemental composition to that of BGH01, the solid-state 11 B NMR revealed that both compounds possessed significant structural differences, which explained for their differences in photocatalytic activity (Additional file 1:Table S3 and Fig. S12).
In light of the moderate photocatalytic activity of BMH01 and BGH01 (Fig. 7), further synthesis optimization was performed to expand their light absorption spectrum into the visible light region. Previous literature showed that increasing the composition of the hexamethylenetetramine precursor (as a carbon source) could modulate the bandgap and photoluminescence properties of BCNO. Based on these reports, BMH and BGH compounds with a higher ratio of hexamethylenetetramine were prepared accordingly while keeping the other parameters constant. The optimized BCNO with a higher carbon content is denoted as BMH03 and BGH03, in which the molar ratio of carbon source was increased from 0.1 to 0.3. The higher ratio of hexamethylenetetramine precursor yielded BMH03 with a higher composition of the graphitic domain as in sp 2 C = C, and a small peak emerged which corresponded to BCN bonding at 191 eV binding energy (Additional file 1:Fig. S7). The increase in the graphitic sp 2 C = C domain upon increasing the concentration of hexamethylenetetramine is consistent with the role of hexamethylenetetramine as both a C and N source in the synthesis of N-doped graphite [66]. The increased sp 2 C = C graphite bonding in BMH03 was further confirmed via 13 C CP-MAS NMR with the emergence of a more prominent peak centered at 40.2 ppm, which is the signature of graphitic C = C(H) bonding (Additional file 1:Table S4).
Optical Properties
The optical properties of BMH and BGH were investigated using UV–visible absorption and photoluminescence spectroscopy, as shown in Fig. 6. Since BGH and BMH series possessed distinctively different structures, and the optical properties of nanomaterials are highly correlated with their structures, the origin of absorption and luminescence for both series were also found to be different. In this study, BGH01 quasi-spherical nanoparticles showed a featureless UV–vis spectrum. (Fig. 6a, red trace). As the ratio of hexamethylenetetramine increased, the intensity of absorbance peaked at 237 nm for BGH03 and increased with the emergence of an additional broad absorption peak centered around 330 nm (Fig. 6a, blue trace). The origin of the optical properties of BCNO is controversial due to the lack of structural analysis of BCNO nanomaterials. The most widely cited origin of photoluminescence of BCNO is attributed to the formation of B, C, N, and O self-interstitial sites, substitutional impurities, and native point defects within hBN or the graphene matrix [50, 67, 68]. Other possible photoluminescence mechanisms in the BCNO system include the electronic transition from the nitrogen-vacancy (VN ) levels to the carbon impurity levels, the electronic transition between the closed-shell BO − and BO 2− anions, and intrinsic state emission and defect state emission (surface energy traps). The featureless UV absorbance of BGH01 can be attributed to the electronic transition between the valence band (VB) and conduction band (CB) of boron nitride with a bandgap energy of ca. 5.9 eV. The lower energy absorption in BGH03 was a result of the mid-gap absorption from the valence band to the nitrogen-vacancy (VN ) level located approximately 0.7–1.0 eV below the conduction band of hBN.(62) The absorption peak at ca. 330 nm could be attributed to the presence of C-related impurities level located ca. 2–4 eV below the conduction band of hBN [69,70,71]. Under 365 nm excitation, BGH01 produced a broad emission with three bumps located at 412 nm, 445 nm, and 489 nm, respectively. Based on the BGH structural analysis, in which the dominant structure was composed of BN and BO-related bonding, the photoluminescence of the BGH series could be most likely originated from the B-O luminescence centers [24, 47, 72]. The yellow-green emission at 445 and 489 nm could be induced by the transition from the VN level to the carbon-related and oxygen defect levels (2–4 eV) below the conduction band of h-BN [69,70,71]. As the C composition increased in BGH03, the emission wavelength was further red-shifted to 506 nm, consistent with literature reports [73, 74]. The stacked photoluminescence (PL), UV absorbance, and Tauc plot for different BGH series prepared in this study are presented in Additional file 1:Fig. S14.
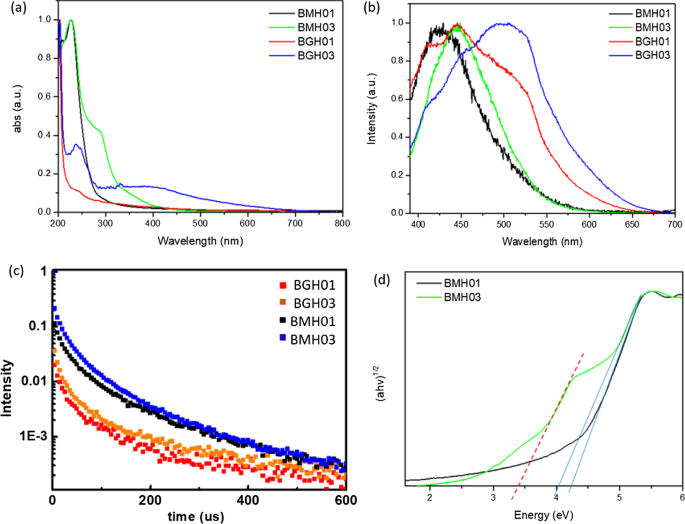
a Overlay UV absorbance spectra of BMH01, BMH03, BGH01, and BGH03. b Stacked photoluminescence spectra of BMH01, BMH03, BGH01, and BGH03 upon excitation at 365 nm c stacked photoluminescence lifetime decay spectrum of BMH01, BMH03, BGH01, and BGH03 monitored at a predetermined λ max for each sample. Samples were excited with 337 nm laser pulses at 298 K, d Overlay Tauc plot (αhv) 1/2 vs. hv, for BMH01 (black trace) and BMH03 (green trace). The optical band gap is represented by thesolid line, while the interband state for BMH03 is represented by the red dashed line
Based on XRD and various spectroscopic analyses, the structure of BMH was deduced to be dominated by BCNO-doped graphene oxides (Fig. 4, Additional file 1:Fig. S7, and Fig. S12, and Table S4). Thus, the optical properties of the BMH series are hypothesized to be more closely related to the carbon-quantum dot (CD) [75, 76] and doped-graphene oxides systems [44, 77,78,79]. Based on the origin of photoluminescence of the CD and graphene oxides, the optical properties of BMH prepared in this study can be attributed to the intrinsic state emission [76, 80, 81], electron–hole recombination [82, 83], and defective state emission [84]. Intrinsic emission of BMH is speculated to have originated from isolated sp 2 luminescence centers embedded within the sp 3 matrix of the carbonaceous film. The sp 3 matrix of graphene oxides is composed of C–OH, C–O–C, and C = O edge sites, whose energy levels lie between the energy levels of π–π* states of the sp 2 C = C domain, thus giving rise to multiple absorption bands. Both BMH01 and BMH03 possessed a strong UV absorbance band at ca. 240 nm, corresponding to the π to π* transition of C = C within the graphene oxides domain. With the increasing ratio of hexamethylenetetramine in the BMH03 sample, an additional bump at 288 nm emerged, which can be ascribed to the n-π* transition of the C = O and C = N bonds of the oxidized graphitic region [77, 85, 86]. The latter absorbance band at ca. 288 nm was induced by oxygen, nitrogen, and boron defect sites, creating new radiative recombination sites [82, 87,88,89]. Upon photoexcitation at 365 nm, BMH01 and BMH03 exhibited a maximum emission wavelengths at 429 and 447 nm, respectively. The BMH03 sample showed a slight red-shift emission, unlike BMH01 due to the greater extent of graphitization [77, 84] (Additional file 1:Figs. 5 and 6). Both BMH samples revealed a broad and much lower energy emission wavelengths than BGH samples due to lower energy emissive centers arising from O, N, and B defects and surface states. According to the electron–hole recombination mechanism, these photoexcited electrons from each defect state recombine with their corresponding holes in the HOMO, thus yielding a broad photoluminescence emission [90] (Fig. 6b). Interestingly, only BMH01 exhibited a pronounced excitation-dependent photoluminescence as observed in other BCNO [72] and carbon quantum dot systems [76]. The presence of O, and N impurities embedded within the graphene oxides matrix was shown to create a large number of surface emissive traps that corresponded to a diverse energy levels within the bandgap, thus yielding an excitation dependent fluorescence spectra in BMH01 (Additional file 1:Fig. S15). In contrast, the lack of an excitation dependent emission in BMH03 could be explained by the formation of a greater extent of graphitization (C = C) with a concurrent reduction in the surface states population (eg.:C = O) [44].
The bandgap values of BMH and BGH prepared in this study were estimated from Tauc's formulation:(αhν) 2 − hν, where α is the absorbance (Fig. 6d). The bandgap was estimated by extrapolating the photon energy intercept at (αhν) 2 = 0. For the BMH series, the presence of multiple energy levels within the optical bandgap may have originated from the electronic transition from various π-π* (C = C bonds) and n-π* of C = O or other surface groups [76, 82, 87]. As for the BGH series, carbon substituted on boron sites (CB ), nitrogen-vacancy sites (VN ), and interstitial carbon defect levels gave rise to the emergence of interband states between the bandgap of hBN. The presence of multiple energy levels was supported by the photoluminescence spectra of lower energy radiative recombinations [24, 47, 66] (Fig. 6b and Table 2). The BGH03 sample exhibited two large bandgaps at 5.7 eV and 3.8 eV, corresponding to the bandgap of hBN and the transition from the valence band to VN levels, respectively [50, 74] (Additional file 1:Fig. S14).
Long-lived charge carriers that can persist into the microseconds and milliseconds timescales in semiconductor photoelectrodes such as CN photocatalysts, have been proposed as an important parameter in enhancing photocatalytic activity by reducing charge recombinations [91,92,93,94,95]. Time-resolved photoluminescence (TRPL) experiments were conducted to gain insight into the recombination processes of the photogenerated charge carriers of BCNO (Fig. 6c). The µs-PL decay kinetics could be fitted with three exponential decays according to the following equation.
$$I\left( t \right) =I_{1} \exp ( - t/\tau_{1} ) + I_{2} \exp ( - t/\tau_{2} ) + I_{3} \exp \left( {t/\tau_{3} } \right)$$The multiple exponential decays imply that BCNO undergoes complex recombination from both intrinsic and defect states of BCNO [32, 72]. In the equation, I 1 through I 3 are constants with values of emission intensity measured at t =0, andτ 1 through τ 3 are the lifetimes of three channels responsible for the decay, respectively. Through multiexponential fitting of the entire decay curves for the BMH and BGH series, the average lifetimes were calculated to be 1.58, 2.10, 5.18, and 8.14 µs for BGH01, BGH03, BMH01, and BMH03, respectively. The values of I and τ in Eq. 1 for the BMH and BGH series are reported in Additional file 1:Table S5. The persistent lifetime of the charge carrier in the BCNO system has been attributed to the presence of shallow traps composed of nitrogen-vacancy (VN ) stabilized by carbon impurities, which were located ca. 0.7 eV-1.0 eV below the conduction band of h-BN [72, 74]. Shallow traps in CN photocatalysts have been attributed to charge separation states with long life-times due to chemical defects [95]. According to works related to prolonged photoluminescence in CN and other nanostructured photoelectrodes [91, 92], the microseconds lifetimes of BCNO-doped graphene oxides and BCNO-doped hBN are associated with the enhanced charged separation within the BCNO domain. The ultralong lifetimes are speculated to be a critical factor in facilitating heterogeneous photocatalysis [91].
Photocatalytic Dye Degradation
As a proof of concept demonstration, the photocatalytic performance of BMH and BGH was evaluated by the photodegradation of methylene blue (MB) under UV–visible light irradiation. Details of the experimental procedure and analysis of the photocatalytic dye degradation are available in the ESI. Figure 7 shows the percent degradation (C /C 0 × 100%) for BMH03 (red line), BMH01 (blue line), BGH01 (green line), BGH03 (orange line), and CN (purple line), where C is the concentration of MB at a time, t and C 0 is the initial concentration MB after the dark equilibrium. According to the Langmuir–Hinshelwood model, ln(C /C 0 ) = kt , where k is the rate constant, the dye degradation rate constant values were calculated to be 2.31 × 10 −3 min −1 for BMH03, 1.52 × 10 −3 min −1 for BGH01, 1.48 × 10 −3 min −1 for BMH01 and 9.38 × 10 −4 min −1 for BGH03. Compared to the state-of-the-art metal-free photocatalyst, BMH03 exhibited a 25% improvement in the photocatalytic dye degradation rates (Fig. 7). This proof-of-concept demonstration warrants a more in-depth investigation of the structure–property relationship of this new metal-free, boron-based photocatalyst.
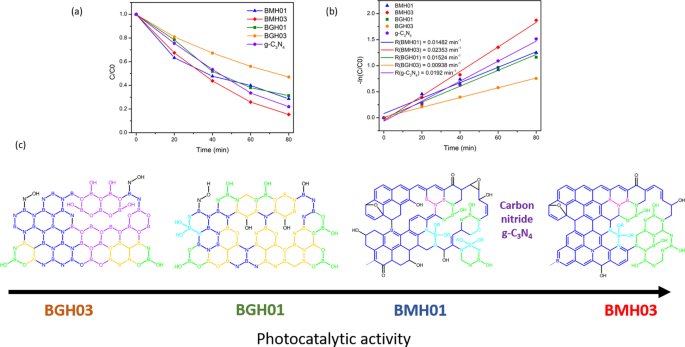
UV–visible light-induced photocatalytic MB degradation using BGH and BMH. a Photodegradation of MB under UV–visible light (plot of C /C 0 ) and b pseudo-first-order rate reaction kinetics for MB dye using BGH, BMH, and CN as a photocatalyst. c The proposed structures for BGH01, BGH03, BMH01, and BMH03 and their corresponding activities toward photodegradation of MB dye. Each domain is color-coded, i.e., BCNO (orange), h-BN and graphene oxides (blue), tricoordinate boron BN2 (OH) and BO2 (OH) (green), boroxol ring (purple), tetracoordinate B sites (aqua blue), and functional groups or dangling bonds (black).
Based on the detailed structural analysis and the proposed structure in Fig. 7c, the highest photocatalytic activity of BMH03 consisted of BCNO-doped graphene oxides [1, 65]. This ternary metal-free photocatalyst is reported to enhance the photocatalytic performances by increasing the charge separation and migration to the reaction site [1]. Additionally, the incorporation of boron into graphene-based materials [11, 20], CN [21, 96], and carbon nanotubes [97] has also exhibited enhanced performance compared to their pristine material without a dopant due to multiple synergistic effects. The large differences in electronegativity between boron, carbon, and nitrogen (2.04 vs. 2.55 vs. 3.04, respectively) yielded a strongly polarized bonding towards C and N atoms. As a result, a local positive charge was formed on boron that turned boron into a strong acidic defect site for preferential adsorption sites of pollutants [98], O2 [97], HOO
−
and OH
−
[99, 100]. Therefore, electron-rich pollutants such as MB (used as a model reaction) were speculated to preferentially adsorbed onto the electropositive B sites of the BMH photocatalyst. The photocatalytic degradation of MB on BCNO was proposed to undergo an indirect dye degradation mechanism [101]. In the indirect photodegradation mechanism, the photogenerated holes on the surface of BCNO produced highly oxidative hydroxyl radicals and attack the 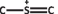 bond of MB. Meanwhile, photogenerated electrons from the conduction band of BCNO formed highly reducing superoxide radical anion O2
−
species that could directly attack MB. Figure 8 illustrates the proposed mechanism of BCNO in photocatalyzing the degradation of MB
bond of MB. Meanwhile, photogenerated electrons from the conduction band of BCNO formed highly reducing superoxide radical anion O2
−
species that could directly attack MB. Figure 8 illustrates the proposed mechanism of BCNO in photocatalyzing the degradation of MB
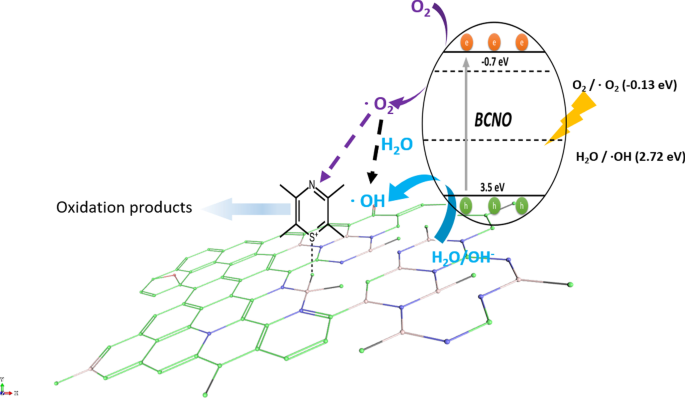
Schematic illustration of the proposed mechanism of BCNO in catalyzing the degradation of MB upon light irradiation. The positively charged MB was selectively absorbed on the N2 B-OH sites. The band structures of BMH03 were determined via UPS and Tauc plot (Fig. 6 and Additional file 1:Fig. S17). The redox potentials of O2 /O2 = − 0.13 eV vs ENHE and H2 O/OH = 2.72 eV vs. ENHE are given in black dashed lines as reference
According to the XPS and solid-state NMR analyses, BMH03 possessed a higher composition of graphitic sp 2 C = C with a simultaneous reduction in tetracoordinate B site compared to BMH01 (Additional file 1:Fig. S9 and Table S4) The high composition of tetracoordinate B-sites in BMH01 (33%) also translated to a reduction in the number of boron Lewis acid sites serving as the active catalytic center, which explains the trend of photocatalytic activities among the BMH series [13]. However, the BGH series comprised the C, and O-doped h-BN domain with various tri- and tetracoordinate boron sites. Interestingly, BGH01 annealed at a lower temperature (Table 1, BGH01LT) was found to be inactive but exhibited a high absorbing ability in removing dye from the solution (Additional file 1:Fig. S1 for TEM morphology; Fig. S16 for photodegradation MB UV–vis absorbance).
The previous report also concluded that BCNO was photocatalytically inactive towards dye degradation but exhibited an excellent absorbing ability in removing dye from the solution [102]. The inactive BGH01LT was comprised primarily of tetracoordinate B sites and boron oxides-related bonding. Based on the SOLA analysis and the literature , the tricoordinate boron site with a δ iso of 16.7 ppm was related to boroxol rings (B2 O3 ) [54, 56]. Our results are also supported by other works on the catalytic activation of peroxymonosulfate using amorphous boron [22]. However, the photocatalytic active BGH01, BMH01, and BMH03 possessed a high composition of BN(OH)2 and BN2 OH bonding sites. Our investigation suggested that the photocatalytic activity of BCNO is highly dependent on the local structure of the boron site. While the exact catalytic site and mechanism are yet to be explored, we proposed that BNx (OH)3−x served as one of the BGH and BMH series catalytic sites. For the BMH series, the formation of tetracoordinate B-O sites was detrimental in catalyzing dye degradation due to the reduction in the Lewis acid site. At the same time, the increasing composition of the sp 2 C = C graphitic domain enhanced the photocatalytic activities of the BGH and BMH series.
Conclusions
In summary, BCNO structures and their photocatalytic activities have been presented here and found to be highly dependent on the choice of precursor, precursor ratios, annealing temperatures, and times. In this study, two types of distinctly different BCNO nanostructures were prepared via low-temperature annealing (600 °C–800 °C):(1) BCNO-doped boron nitride and (2) BCNO-doped graphene oxides. Through systematic investigation of using two different nitrogen precursors, crystalline BCNO with a quasi-spherical shape was prepared at 800 °C for 12 hr using guanidine hydrochloride as the nitrogen source. This series of BCNO exhibited moderate photocatalytic activity through the emergence of BN2 (OH) or BN(OH)2 tricoordinate boron serving as the Lewis acidic site. However, BCNO prepared using melamine as the nitrogen source at 600 °C yielded multi-layered sheets with ill-defined shapes. These BCNO-doped graphene oxides layered structures exhibited the highest photocatalytic activity, surpassing the state-of-art metal-free photocatalyst, CN. For the melamine-derived BCNO layered structures, the presence of tricoordinate boron species as BN2 (OH) or BN(OH)2 and a higher composition of graphitic sp 2 C = C were speculated to play an important role in promoting their photocatalytic activity. This study demonstrates the potential of BCNO as a photocatalyst for energy conversion and environmental remediation applications. Further structural optimization on this new B-C-N–O photocatalyst system is expected to facilitate the development of a sustainable catalyst for applications including solar hydrogen fuel production, environmental remediation, electrocatalytic oxygen reduction reaction, and catalytic oxidative dehydrogenation reaction.
Availability of Data and Materials
All data are fully available without restriction.
Abbreviations
- BCNO:
-
Boron carbon oxynitride
- CN:
-
Carbon nitride
- hBN:
-
Hexagonal boron nitride
- TRPL:
-
Time-resolved photoluminescence
- MAS:
-
Magic angle spin
- CP:
-
Cross polarization
- SOLA:
-
Solid line shape analysis
- I :
-
Intensity
- ATR:
-
Attenuated total reflectance
Nanomateriales
- Fibra de carbono
- Detector de monóxido de carbono
- Papel carbón
- Carbono M2
- Los nanotubos de carbono superan el límite de la electrónica flexible
- Creación y generación de imágenes de ciclocarbono
- Imagen de carbono oceánico en escala atómica
- Hilo de nanotubos de carbono, músculo y láminas transparentes
- ¿Qué es la fibra de carbono?
- ¿La fibra de carbono es conductora?
- Acero al carbono frente a acero inoxidable



