Detección de peróxido de hidrógeno basada en la modificación de superficies internas de nanoporo de estado sólido
Resumen
Existen muchas técnicas para la detección de moléculas. Pero la detección de moléculas a través de nanoporos de estado sólido en una solución es una de las tecnologías prometedoras, de alto rendimiento y de bajo costo que se utilizan en la actualidad. En la presente investigación, se fabricó una plataforma de nanoporos de estado sólido para la detección de peróxido de hidrógeno (H 2 O 2 ), que no solo es un producto sin etiqueta, sino también un participante significativo en la reacción redox. Hemos fabricado con éxito nitruro de silicio (Si 3 N 4 ) nanoporos con diámetros de ~ 50 nm mediante el uso de un haz de iones de Ga enfocado, la superficie interna del nanoporo se ha modificado con peroxidasa de rábano picante (HRP) empleando la química de acoplamiento de carbodiimida. Las enzimas HRP inmovilizadas tienen la capacidad de inducir reacciones redox en un solo canal de nanoporos. Además, un único ABTS agregado en tiempo real • + Se monitorearon e investigaron los eventos de translocación molecular. El biosensor de nanoporos de estado sólido diseñado es reversible y se puede aplicar para detectar H 2 O 2 varias veces.
Antecedentes
La tecnología de detección de nanoporos se origina en el contador Coulter [1] y el canal de iones de la celda [2]. Nanopore detecta moléculas cargadas presentes en una solución que lo atraviesa. La aparición de las moléculas en nanoporo puede cambiar la conductancia del poro aparentemente, en consecuencia un cambio en la señal de corriente. El cambio en la corriente proporciona la información sobre los tamaños y la concentración de las moléculas dentro del poro, para revelar el proceso dinámico de los comportamientos de translocación de las moléculas [3]. Algunos objetos a nanoescala se pueden detectar utilizando un nanoporo, como nanopartículas [4,5,6], virus [7,8,9], moléculas de proteínas [10,11,12,13] y secuencias de ADN [14,15,16 , 17]. Los nanoporos son de dos tipos. Nanoporo de biología y nanoporo de estado sólido. El nanoporo biológico tiene una relación señal / ruido (SNR) más baja y una resolución más alta. Las proteínas pequeñas y desplegadas se pueden detectar mediante el uso de nanoporos biológicos [18,19,20,21,22,23]. El nanoporo de estado sólido es de tamaño ajustable y tiene una mayor estabilidad. El nanoporo de estado sólido normalmente se perfora en una película, esta película divide la celda fluídica en dos partes [24]. Se aplica un voltaje polarizado a través de una membrana delgada que contiene un nanoporo, lo que genera una corriente iónica de una celda a otra [25]. Las moléculas de proteína, incluidas las estructuras plegadas y desplegadas, se detectan y analizan mediante nanoporos de estado sólido [26,27,28,29]. La interacción de proteínas también se puede detectar utilizando nanoporos de estado sólido [30, 31]. Además, tiene la capacidad de detectar la cinética de las proteínas [32, 33]. Para resolver los límites en el rango de detección, se han aplicado extensivamente nanoporos de estado sólido químicamente modificados [34,35,36,37,38,39], se han aplicado nanoporos de estado sólido químicamente modificados para detectar ADN monocatenario [40] y proteínas [41].
Ya se han aplicado muchos métodos cuantitativos para la detección de H 2 O 2 , la mayoría de ellos se basan en espectrometría [42,43,44,45], quimioluminiscencia [46,47,48,49], amperometría [50,51,52,53] y electroquímica [54,55,56,57] . Los métodos convencionales de espectrometría y quimioluminiscencia suelen consumir mucho tiempo y son costosos. El sensor de nanoporos de estado sólido tiene bajo consumo y estructura simple, y puede usarse para detectar moléculas pequeñas.
A continuación, presentamos un tipo nanoporo en estado sólido que fue modificado con peroxidasa de rábano picante (HRP). Los HRP se inmovilizaron en la superficie interna del nanoporo de estado sólido, los HRP inmovilizados permanecieron activos en la reacción redox que se produjo dentro de un solo canal de nanoporos en presencia de H 2 O 2 [58]. El ABTS • + producido en la reacción redox se agregaría, entonces el ABTS agregado • + pasó a través de nanoporos. Los eventos de translocación se pueden detectar. Para la detección de peróxido de hidrógeno, la estructura del estado sólido es simple y puede detectar el ABTS agregado • + mediante el uso de bajo consumo de reactivo. Este nanoporo de estado sólido de modificación de enzimas de peroxidasa de rábano picante (HRP) puede lograr el peróxido de hidrógeno (H 2 O 2 ) detectando indirectamente, a través del ABTS agregado • + detección. Tiene un significado instructivo para la detección de moléculas individuales y el ensamblaje de moléculas en nanoporos de estado sólido interno.
Métodos
Productos químicos y materiales
La molécula de peroxidasa de rábano picante (HRP) (1 mg mL -1 , Comisión de Enzimas No 1.11.1.7, 44 kDa) se adquirió de Xiya Reagent (Chengdu, China). La muestra (HRP) se disolvió en 0,02 µm de PBS 0,1 M filtrado, se almacenó a 4ºC y se empleó en los dos días siguientes a la preparación. Cloruro de potasio (KCl), N- (3-dimetilaminopropil) -N'-etilcarbodiimida (EDC), N-hidroxisuccinimida (NHS) y ácido 2,2'-azino-bis (3-etilbenzotiazolina-6-sulfónico) ((ABTS) ), 98%) se adquirieron de DiBo chemical technology co., LTD (Shanghai, China). Peróxido de hidrógeno (H 2 O 2 , 30%) se compró de Sinopharm Chemical Reagent Co., Ltd. (3-Aminopropil) trietoxisilano (3-APTES) se adquirió de Sigma-Aldrich (St. Louis, MO, EE.UU.). Los experimentos se realizaron utilizando agua no purificada de un sistema de purificación de agua Milli-Q (resistividad de 18,2 MΩ / cm, 25 ° C, Millipore Corporation, Billerica, MA, EE. UU.) Y se filtró a través de 0,02 μm en un sistema FEI Strata 201 FIB (FEI Co., Hillsboro, OR, EE. UU.), Un Zetasizer (Malvern Zetasizer Nano ZS) y un Axopatch 700B (Molecular Devices, Inc., Sunnyvale, CA, EE. UU.). Las imágenes de nuestros instrumentos usados se agregaron al material complementario (consulte el archivo adicional 1:Figura S1).
Fabricación de nanoporos de estado sólido y mediciones eléctricas
Primero, una fina membrana de Si 3 N 4 (100 nm de espesor) se depositó sobre un sustrato de Si que tenía 300 µm de espesor. Seguido de fotolitografía (el tamaño de la ventana abierta es 500 × 500 μm 2 ). Luego, la superficie de la membrana se bombardeó con iones Ga + usando un sistema FEI Strata 201 FIB (FEI Co., Hillsboro, OR, EE. UU.) A un potencial de aceleración de 30 kV, mientras que la corriente se midió como 1 pA. El tiempo de molienda fue de 1,5 s en modo puntual. Finalmente, se obtuvieron los chips de nanoporos de estado sólido y se limpiaron en una solución de piraña recién preparada a 80 ° C durante 30 min, seguido de un enjuague con agua ultrapura. Después de la limpieza, el chip se ensambló en una celda de teflón hecha a medida con dos juntas tóricas de Viton para separar los dos lados del chip y formando dos depósitos para garantizar el único camino para la corriente iónica a través del nanoporo. Las imágenes de nuestros aparatos usados se agregaron al material complementario (consulte el archivo adicional 1:Figura S2). Se conectaron electrodos (Ag / AgCl) a la celda fluídica y a un amplificador de pinza de parche (Axopatch 700B, Molecular Devices, Inc., Sunnyvale, CA, EE. UU.) Que hizo que la corriente iónica fuera medible bajo voltajes constantes, con una frecuencia de muestreo de 100 kHz para señales. . El filtro Bessel de paso bajo de ocho polos interno del amplificador se fijó en 10 kHz [3]. Todo el instrumento se colocó en una caja de doble jaula de Faraday.
Resultados y discusión
Inmovilización de Nanopore con HRP
El nanoporo seleccionado con un diámetro de ~ 50 nm se sumergió en una solución de piraña a 80 ° C durante 30 min. Después de tratar con solución de piraña, la superficie interna del nanoporo pudo tomar grupos hidroxilo de silicio. Posteriormente, se activó toda la película fina con (3-aminopropil) trietoxisilano (3-APTES). Como resultado del tratamiento con 3-APTES, el amino (-NH 2 ) grupos se generaron en la superficie de la película.
Después de la activación con (3-aminopropil) trietoxisilano (3-APTES), el chip de nanoporos se llevó a una solución de PBS 0,1 M de N- (3-dimetilaminopropil) -N'-etilcarbodiimida (EDC) (10 mM) y N-hidroxisuccinimida ( NHS) (20 mM). Posteriormente, el chip de nanoporos se introdujo en peroxidasa de rábano picante (HRP) (10 ng / ml). De acuerdo con resultados de investigaciones previas de nuestro grupo [3], con diferentes concentraciones de sal de 0.1 a 2 M KCl, pH 7.0, el HRP no se agregó. A causa del pI siendo el valor de la peroxidasa de rábano picante de 4,3 ± 0,2, también probamos que el HRP no se agrega en KCl 0,1 M pH 6,0 y pH 7,0. El reactivo EDC activó los grupos carboxilo (-COOH) de HRP en un intermedio de o-acilisourea altamente reactivo. Además, el intermedio se convirtió en un éster reactivo con succinimidilamina más estable en presencia de NHS [58]. Como resultado, en el acoplamiento covalente del intermedio con el (-NH 2 ) generado en las superficies internas del nanoporo para formar enlaces amida estables (Fig. 1).
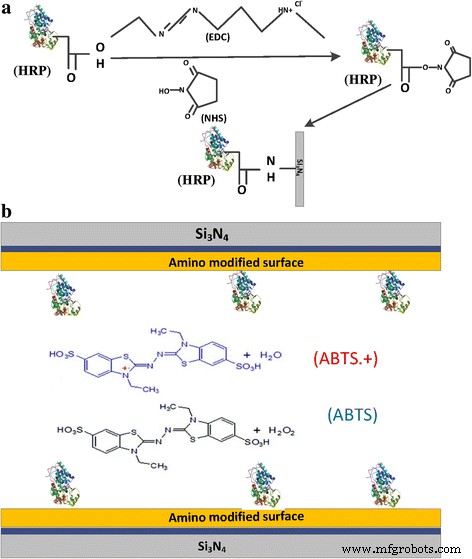
Realización de proceso de modificación en un único canal de nanoporos de estado sólido. un Representación esquemática de la unión covalente de peroxidasa de rábano picante (HRP) a un solo canal de nanoporos a través de la química de acoplamiento de carbodiimida. Los grupos carboxilo (-COOH) de HRP se activaron mediante una solución de EDC, lo que permitió que el HRP reaccionara con (-NH 2 ) generado en la superficie de un chip de nanoporos. b Esquema del sensor de peróxido de hidrógeno de HRP inmovilizado, la superficie interna del sensor se modificó con HRP. Cuando H 2 O 2 y ABTS ocurrió, el ABTS • + producido. La estructura cristalina de HRP se utilizó con el permiso del autor [3]
Estos procesos nos llevan hacia la inmovilización de HRP en la superficie interna de un solo nanoporo. La realización del proceso de funcionalización se confirmó midiendo la corriente-voltaje ( I-V ) de un solo nanoporo antes y después de la modificación (Fig. 2).
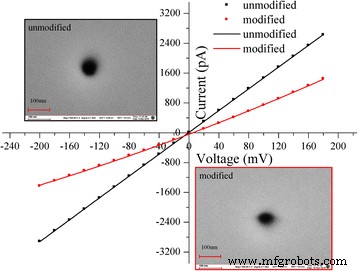
Realizando una corriente-voltaje típica ( I-V ) curvas del nanoporo no modificado (original) y modificado en KCl 0,1 M, tamponado a pH 7,0 con PBS 0,1 M. La línea negra es el I-V curvas de nanoporos sin modificar y línea roja es el I-V curvas de nanoporo modificado con HRPs. Las inserciones son la microscopía electrónica de barrido (SEM) de un solo nanoporo (diámetro de ~ 50 nm cis) y el sensor de nanoporos. 100 nm es escala
Caracterización de nanoporos de estado sólido modificado HRP
Aquí, la forma de un solo Si 3 N 4 El canal de nanoporos es cilíndrico. La Figura 2 muestra la corriente-voltaje típica ( I-V ) curvas del nanoporo no modificado (original) y modificado en KCl 0,1 M, tamponado a pH 7,0 con PBS 0,1 M. Después de modificar la superficie interna del nanoporo con enzimas HRP, el tamaño de los poros se hizo más pequeño.
Según Wanunu et al, teniendo en cuenta la conductancia del exterior del nanoporo, el diámetro del nanoporo en estado sólido se puede calcular mediante la siguiente ecuación:
$$ d =\ left (1+ \ sqrt {1+ \ frac {16 \ sigma l} {\ pi G}} \ right) G / 2 \ sigma $$ (1)Dónde, d y l son el diámetro y la longitud del poro, G es la conductancia de poros abiertos de nanoporos, σ es la conductividad de la solución de iones.
Teniendo en cuenta los efectos geométricos, después de la modificación de nanoporos en estado sólido con enzimas HRP, se puede calcular el tamaño efectivo. El diámetro de un solo nanoporo se puede calcular basándose en la ecuación (1). Donde, el valor de conductancia ( G sin modificar ) es ~ 15 nS se puede obtener de I-V curvas del nanoporo de estado sólido sin modificar. La conductividad ( σ ) de solución iónica de KCl 0,1 M (25 ° C), tamponada a pH 7,0 con PBS 0,1 M es ~ 1,28 S / m. Por lo tanto, el diámetro del nanoporo no modificado es ~ 51 nm, es similar al diámetro medido. Utilizando el mismo método, el valor obtenido de conductancia ( G modificado ) es ~ 7,5 nS, y se puede calcular el diámetro (~ 34 nm) del nanoporo modificado. La reducción en el diámetro es posible debido a las siguientes dos razones, primero es tratar la superficie interna del nanoporo con (3-aminopropil) trietoxisilano (3-APTES), permitiendo que la superficie del nanoporo tome (-NH 2 ) grupos amino. La segunda razón es que el diámetro hidrodinámico ( D h ) de la enzima HRP es ~ 8 nm [3], las HRP inmovilizadas podrían reducir el diámetro de los poros. Aquí, el nanoporo de estado sólido modificado con HRP con un diámetro de ~ 34 nm se utiliza como canal de detección de peróxido de hidrógeno.
El principio de la reacción redox
La reacción redox se llevó a cabo dentro de un único nanoporo modificado, y el siguiente proceso de reacción presentado concuerda bien con la reacción redox propuesta [58]. En presencia de H 2 O 2 (0,5 mM), las enzimas HRP inmovilizadas en la superficie interna del nanoporo se convirtieron en el compuesto 1 inmediatamente. Luego, el compuesto 1 aceptó un electrón de la molécula de sustrato reductor ABTS (1,5 mM) para generar el compuesto 2. Posteriormente, el compuesto 2 se redujo de nuevo a la enzima en reposo mediante una transferencia de electrones de otra molécula de sustrato ABTS.
Los productos catiónicos (ABTS • + ) de las reacciones redox se acumularon en un solo nanoporo. La translocación de moléculas acumuladas del canal de nanoporos cambiaría la conductancia ( G ), y por lo tanto el cambio de corriente ( ΔI b ) se puede encontrar.
$$ \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {3 +} \ right) \ mathrm {Porp} + {\ mathrm {H}} _ 2 { \ mathrm {O}} _ 2 \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) {\ mathrm {Porp}} ^ {\ cdotp +} \ left (\ mathrm {Compuesto} \ 1 \ right) + {\ mathrm {H}} _ 2 \ mathrm {O} $$ $$ \ mathrm {H} \ mathrm { R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) {\ mathrm {Porp}} ^ {\ cdotp +} + \ mathrm {ABTS} \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {4 +} =\ mathrm {O} \ right) \ mathrm {Porp} \ left (\ mathrm {Compuesto} \ 2 \ right) + {\ mathrm {ABTS}} ^ {\ cdotp +} $$ $$ \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe }} ^ {4 +} =\ mathrm {O} \ right) \ mathrm {Porp} + \ mathrm {ABTS} \ to \ mathrm {H} \ mathrm {R} \ mathrm {P} \ left ({\ mathrm {Fe}} ^ {3 +} \ right) \ mathrm {Porp} + {\ mathrm {ABTS}} ^ {\ cdotp +} + {\ mathrm {H}} _ 2 \ mathrm {O} $$Detección de eventos de translocación
Los experimentos se realizaron utilizando nanoporos modificados con peroxidasa de rábano picante (HRP) con diámetros de poros modificados (~ 34 nm) en KCl 0,1 M, tamponado a pH 7,0 con PBS 0,1 M. 2, 2'-Azinobis- (3-etilbenztiazolina-6-sulfonato (ABTS) (1,5 mM) y peróxido de hidrógeno (H 2 O 2 ) (0,5 mM) al compartimento trans del nanoporo. Después de agregar ABTS y H 2 O 2 , se realizaron los experimentos utilizando voltajes polarizados de -100 a -800 mV, y se muestrearon a 100 kHz. No hubo ningún evento de translocación hasta que el voltaje aumentó a -400 mV. La Figura 3 muestra trazas de corriente iónica representativas del evento de translocación a diferentes voltajes de -400 a -800 mV en 0.1 M KCl, 0.1 M PBS, pH 7.0. Los datos de los experimentos de eventos de translocación de larga duración de diferentes voltajes se agregaron al material complementario (consulte el archivo adicional 1:Figura S3).
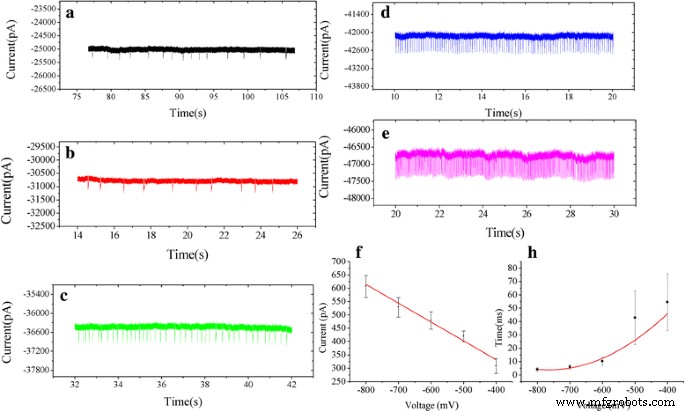
un - e Representación esquemática de los eventos de translocación a diferentes voltajes de -400 a -800 mV. La frecuencia de los eventos de translocación aumentó cuando el voltaje aplicado aumentó de -400 mV a -800 mV. f La amplitud de la corriente aumenta linealmente con el voltaje. h Una función que decae exponencialmente ( t d ~ e −v / v0 ) se empleó para ajustar el tiempo de permanencia en función de los voltajes aplicados
Se observaron los eventos de bloqueo de corriente de milisegundos, realizados en KCl 0,1 M, PBS 0,1 M, pH 7,0. Añadiendo el reactivo H 2 O 2 y ABTS en el transcompartimento, las enzimas HRP se inmovilizaron en la superficie interna del canal de nanoporos individual y se produjo la reacción redox. Abundancia de ABTS • + se produjeron moléculas, una sola molécula más pequeña ABTS • + puede que no se detecte con nuestro nanoporo de estado sólido, debido a la resolución del sistema [3]. Sin embargo, estas moléculas se agregarían después de su producción. Por lo tanto, es posible detectar el ABTS • + moléculas. Aquí, se mantuvieron los voltajes negativos y se agregaron ABTS • + moléculas que pasan a través de los nanoporos. Hubo un flujo electroforético y electroosmótico cuando se aplicó voltaje negativo. La HRP se cargó negativamente en KCl 0,1 M, PBS 0,1 M, pH 7,0 [3], como resultado, se produciría una doble capa eléctrica y la eletroosmosis sería hacia la dirección negativa del electrodo. Por este motivo, la electroforesis y la eletroosmosis se dirigieron en la misma dirección. El ABTS agregado • + en el único canal de nanoporos se transportaría a través del nanoporo de estado sólido, fluiría hacia la dirección negativa del electrodo.
Análisis estadístico de eventos de translocación
Dado que el voltaje polarizado jugó un papel clave en la translocación de ABTS agregado • + , la influencia de los bloqueos actuales de ABTS agregados • + Se discutió el paso a través del nanoporo modificado de HRP frente a los voltajes aplicados. La frecuencia de ocurrencia de eventos de translocación mejoró enormemente con el aumento de voltaje (Fig. 3f). A medida que aumenta el voltaje, también lo hace la amplitud de la corriente. Sin embargo, los eventos de translocación desaparecieron gradualmente cuando el voltaje polarizado se mantuvo por debajo de -300 mV, lo que sugirió que ABTS agregado • + a través de los nanoporos modificados de HRP necesitaban un voltaje de umbral de -300 mV. La Figura 4 muestra histogramas de la amplitud de corriente media de los eventos de translocación medidos para ABTS agregado • + a diferentes voltajes. Según las curvas de ajuste, los valores máximos del bloqueo actual ( ΔI b ) son 308,4 ± 27,795 pA, 419,1 ± 20,354 pA, 478,8 ± 32,857 pA, 528,1 ± 36,98 pA, 606,9 ± 40,916 pA a −400, −500, -600, −700 y −800 mV, respectivamente, es probable que la reducción de la corriente es inducida por ABTS agregado • + molécula que pasa a través del nanoporo a diferentes voltajes. Los valores de amplitud de corriente se ajustaron con una función polinomial de primer orden, que produce una pendiente de −0,706 y una intersección de 49,262. Sin embargo, según las curvas de ajuste, los valores del tiempo de permanencia son 54,5 ± 21,374 ms, 42,8 ± 20,181 ms, 10,3 ± 3,05 ms, 6,0 ± 1,744 ms, 4,0 ± 1,441 ms, en −400, −500, −600, - 700 y −800 mV. La Figura 3h muestra una función que decae exponencialmente ( t d ~ e −v / v0 ) se empleó para ajustar el tiempo de permanencia en función de los voltajes aplicados. Los histogramas del tiempo de permanencia de los eventos de translocación se agregaron al material complementario (consulte el archivo adicional 1:Figura S4).
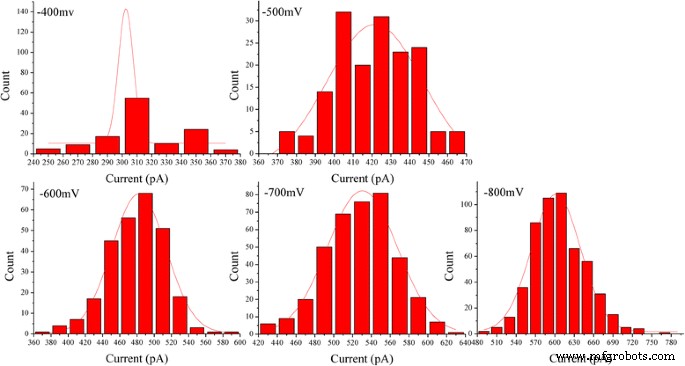
Los histogramas de la amplitud de corriente media de los eventos de translocación medidos para ABTS agregado • + a diferentes voltajes (-400, -500, -600, -700, -800 mV) en 0.1 M KCl, 0.1 M PBS, pH 7.0. Todos los histogramas se ajustaron con distribución gaussiana
El bloqueo actual versus el tiempo de permanencia de los eventos para cada ABTS agregado • + a diferentes voltajes se ajustaron en diagramas de dispersión bidimensionales (Fig. 5). Todos los ABTS agregados • + muestran un grupo de eventos de −400 a −800 mV, los grupos de eventos principales se deben al ABTS agregado • + pasando a través del nanoporo de estado sólido modificado con HRP.
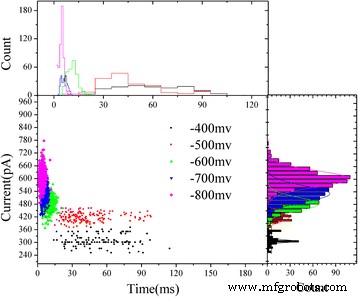
Gráficos de dispersión bidimensionales del bloqueo actual frente al tiempo de permanencia de los eventos para cada ABTS agregado • + a diferentes voltajes. Sus histogramas correspondientes se colocan a la derecha y arriba. Todos los histogramas se ajustaron con distribución gaussiana
Además, se analizó el evento de translocación único en cada voltaje, y el bloqueo de corriente fue inducido por el mismo tamaño y sustancia cargada. Por lo tanto, se considera que cada evento de translocación fue inducido por el único ABTS agregado • + . Analizar el tiempo de translocación de ABTS agregado • + en nuestros experimentos. La duración actual del bloqueo t d se considera el tiempo de permanencia de un único ABTS agregado • + desde el lugar donde se produjo hasta la salida del nanoporo. Aquí, se consideró otra condición, puede haber algunas enzimas HRP inmovilizadas en la entrada del nanoporo y podría catalizar la reacción redox. Por lo tanto, se llevaron a cabo otros experimentos para verificar que la reacción redox se produjera en la superficie interna de un solo nanoporo en lugar de en la entrada. Para la verificación se aplicaron y analizaron los PRH no modificados. Estos nanoporos se activaron con 3-APTES. Y la misma concentración de HRP (10 ng / ml), ABTS (1,5 mM) y H 2 O 2 (0,5 mM) al compartimento trans del nanoporo, el voltaje polarizado negativo se aplicó en KCl 0,1 M, PBS 0,1 M, pH 7,0, debido a la fuerza de electroforesis, los HRP no pudieron pasar a través del nanoporo. Debido a la reacción redox, el ABTS • + agregado producido, pero no se encontraron eventos de translocación. Es posible que el ABTS agregado • + causar un efecto electrostático con HRP y prevenir el ABTS agregado • + pasando a través del nanoporo.
La Figura 6 muestra los diagramas de dispersión bidimensionales del cambio de conductancia ( ΔG ) versus el tiempo de permanencia de los eventos para cada ABTS agregado • + a diferentes voltajes. Se puede encontrar que el cambio de conductancia ( ΔG ) concentrado principalmente en 0,8 nS. La forma de los eventos de translocación es casi la misma. El valor medio de ΔG es ~ 0.8 nS a diferentes voltajes. Se puede especular que la exclusión de volumen de cada ABTS agregado • + La molécula es casi la misma. Es posible que los efectos electrostáticos y estéricos del ABTS agregado • + las moléculas pueden cambiar la corriente iónica. Después del análisis, dos formas típicas de trazas de corriente con el ABTS agregado con carga positiva • + Se observaron translocaciones (Fig. 7). Los eventos de translocación a -700 mV como representante. Se analizó el porcentaje de dos eventos tipo, y se puede observar que el porcentaje de eventos tipo 1 aumentó con el aumento de voltaje, por otro lado, el porcentaje de eventos tipo 2 disminuyó. Se consideró que un voltaje más alto hace que la translocación sea más rápida que el voltaje más bajo.
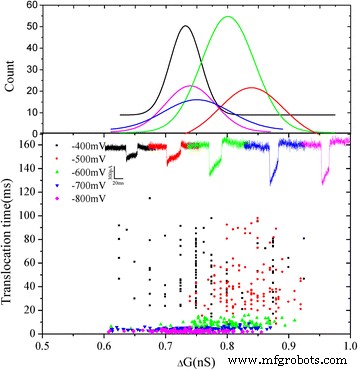
Representación esquemática de diagramas de dispersión bidimensionales de ΔG versus el tiempo de permanencia de los eventos para cada ABTS agregado • + a diferentes voltajes. Las curvas de ajuste correspondientes se colocaron arriba. El insertar son los eventos de translocación de diferentes voltajes (de −400 a −800 mV)
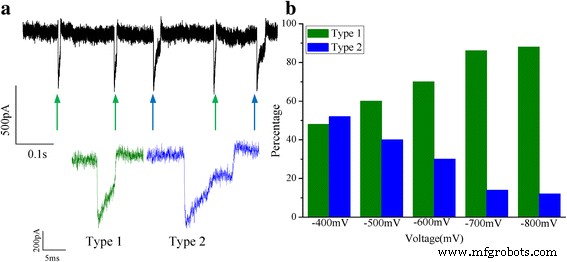
un Esquema de dos tipos de eventos de translocación a un voltaje de -700 mV. b El porcentaje de eventos de dos tipos a diferentes voltajes (−400, −500, −600, −700, −800 mV)
Las señales de bloqueo actuales revelaron el tamaño, la conformación y la interacción de ABTS agregados • + pasando a través del único canal de nanoporos. Para el cambio en la forma actual, se especuló el proceso de los cambios. Para el evento 1, las señales de corriente tienen una parte de fluctuación típica con una intensidad profunda y un tiempo de permanencia corto. Es posible que el ABTS agregado • + pasa a través del nanoporo desde el lugar donde se produce. Cuando el ABTS agregado • + Pasó a través del nanoporo, la corriente iónica del nanoporo se restauró al nivel original (Línea de base) ( I 0 ). Para el evento 2, las señales de corriente tienen una parte de fluctuación con una intensidad profunda y luego tienen una etapa horizontal. Esta forma de señales se puede atribuir a la interacción electrostática de ABTS agregado • + con los HRP a la salida de nanopore, y la corriente se recuperó lentamente hasta la línea de base. Para comprender mejor el cambio actual, debemos comenzar con el cambio de conductancia de poro abierto ( G poro ) a una concentración de sal (KCl 0,1 M). Como se discutió en los estudios anteriores, una ecuación de la conductancia de poros abiertos de un nanoporo cargado negativamente con un diámetro de d y una longitud de l a baja concentración de sal se puede describir como
$$ {G} _ {p ore} =\ frac {\ pi {d ^ 2} _ {p ore}} {4 {l} _ {p ore}} \ left [\ left ({\ mu} _ { K ^ {+}} + {\ mu} _ {C {l} ^ {-}} \ right) {n} _ {K Cl} \ cdot e + {\ mu} _K \ frac {4 {\ sigma} _p } {d_ {p ore}} \ right] $$ (2)donde μ K y μ Cl son las motilidades electroforéticas de K + y Cl - , n KCl es la densidad numérica de K + y Cl - , la carga elemental es e, σ p es la densidad de carga superficial de las superficies de nanoporos. En este experimento, el nanoporo de estado sólido se modificó químicamente y se cambió el diámetro del nanoporo. La densidad de carga superficial de la superficie del nanoporo ( σ p ) no se puede obtener exactamente. Por lo tanto, la conductancia de poros abiertos ( G poro ) se calculó con base en la ecuación (1). Debido a la ecuación (1), la conductancia de poros abiertos ( G poro ) es ~ 7,5 nS. Se especula que el cambio de conductancia puede atribuirse a dos razones [15]. La primera razón es que, el volumen de exclusión de iones en nanoporos fue ocupado por el agregado ABTS • + moléculas. Como resultado, se redujo la conductancia de nanoporos en estado sólido ( ΔG - ). La segunda razón es que, algunos iones fueron traídos del nanoporo por el ABTS agregado • + moléculas que aumentaron la conductancia de nanoporos de estado sólido. En estos experimentos, el ABTS • + producido dentro de nanopore, y no se trajeron iones. Por lo tanto, el cambio en la conductancia de nanoporos de estado sólido ( ΔG ) solo fue inducida por la exclusión de volumen. Entonces, el cambio total de la conductancia se puede describir como
$$ \ varDelta G =\ varDelta {G} ^ {-} $$ (3)La disminución en la conductancia de nanoporos en estado sólido es inducida por la exclusión de volumen y se puede calcular mediante la siguiente ecuación
$$ \ varDelta {G} ^ {-} =\ sigma \ frac {\ gamma \ varLambda} {{\ left (l + 0.8 d \ right)} ^ 2} $$ (4)donde γ es el factor de forma de la partícula, que es la relación de las áreas superficiales del mismo volumen esférico y la partícula. En este trabajo, el ABTS agregado • + molécula se simplificó a un objeto global, por lo tanto, el valor de γ es 1 y Λ es la exclusión de volumen. La conductividad de la solución a granel σ es 1,28 S / m, KCl 0,1 M (25 ° C).
Para la exclusión de volumen ( Λ ), podemos deducir de los eventos de translocación de algunas otras moléculas. Para conectar el cambio de conductancia ( ΔG ) a la propiedad física de las moléculas, la ley de Ohm se puede aplicar al cambio de volumen de la solución de electrolito basada en el nanoporo de estado sólido [59]. Cuando ocurre un evento de translocación de una molécula en un nanoporo cilíndrico de estado sólido, la corriente disminuyó instantáneamente. Cuando la resistencia del nanoporo de estado sólido es la resistencia del circuito completo, el cambio de conductancia ( ΔG ) se puede describir mediante la siguiente ecuación
$$ \ varDelta G (t) =- {G} _ {p ore} \ frac {\ varLambda (t)} {H_ {eff} {A} _p} \ left [1+ f \ left ({d} _m / {D} _p, {l} _m / {H} _ {eff} \ right) \ right] $$ (5)En esta ecuación, A p H ef =V p es el volumen de nanoporos de estado sólido, f ( d m / D p , lm / H ef ) es el factor de corrección (ignoró el efecto de carga superficial), en nuestros experimentos, simplificamos el ABTS agregado • + molécula a un objeto global; por lo tanto, el factor de corrección es 1. La d m / D p es la relación entre el diámetro de la molécula y el diámetro del nanoporo, el lm / H ef es la relación entre la longitud efectiva de la molécula y la longitud efectiva de la naoporo. La expresión (5) se puede simplificar como
$$ \ varDelta G / {G} _ {p ore} \ approx \ varLambda / {V} _p $$ (6)El valor medio de conductancia ( G poro ) ha sido analizado de eventos de translocación. De la ecuación (5), el valor medio de exclusión de volumen ( Λ ) a diferentes voltajes (-400, -500, -600, -700, -800 mV) se pueden obtener. Mientras tanto, se conoce el tamaño del nanoporo utilizado, el volumen del nanoporo ( V p ) es ~ 90746 nm 3 . Debido a la ecuación (4), el valor del cambio de conductancia ( ΔG - ) se puede calcular como ~ 0,6 nS. El valor medio del cambio de conductancia que se obtuvo de los experimentos de eventos de translocación a diferentes voltajes (-400, -500, -600, -700, -800 mV) es ~ 0,784 nS. Se puede encontrar que el valor calculado está cerca del valor experimental.
En alguna investigación previa, se ha logrado detectar moléculas de peróxido de hidrógeno con diferentes tecnologías. Pero es raro detectar peróxido de hidrógeno por nanocanales. Tan y col. [3] señales de eventos dispares diferenciados cuando los HRP se enhebraban en nanoporos, había ABTS y H 2 O 2 en solución de KCl. Los diferentes tipos de señales con translocación de HRP se consideraron ABTS • + pasando a través de nanoporos. Se analizaron seis eventos típicos de la translocación del producto de sustratos de catálisis enzimática. Especulaban sobre el proceso probable de todo tipo. Sin embargo, no hay pruebas suficientes para testificar. Mubarak Ali y col. han logrado detectar los productos de reacción redox internos de nanocanales cónicos individuales [58]. Descubrieron que el radical catiónico ABTS • + reduced the ion current in the HRP-nanochannel in a voltage-dependent fashion, consistent with voltage-dependent concentrations of ions in conical nanochannels. The magnitude of the current blockage was correlated with the H2 O 2 concentration in the solution.
Conclusiones
In conclusion, we fabricated a Si3 N 4 nanopore employing a FIB successfully, a single naonopore system whose surface was modified with covalently linked HRP enzymes. The effect of the immobilized HRPs enzymes in a single solid-state nanopore as a hydrogen peroxide (H2 O 2 ) sensor was affirmed by investigating products (ABTS •+ ) of the redox reactions occurring in presence of the substrates H2 O 2 and ABTS. The aggregated cationic radical ABTS •+ produced inside the solid-state nanopore and reduced the ionic current in the HRPs modified solid-state nanopore, are consistent with voltage-dependence. The current blockade trends showed linear dependence for applied biased voltages. The relationship between the dwell time versus applied biased voltage was the exponentially decaying (t d ~ e −v/v0 ). Meanwhile, the aggregated ABTS •+ passed through the HRPs modified nanopores needed a −300 mV threshold voltage. The change of conductance (ΔG) has been calculated analytically and compared to the measured experimental values. The translocation events were produced by the certain size aggregated cationic radical ABTS •+ . We expect that using solid-state nanopores will allow lowering the detection limit and improve the system sensitivity. For our solid-state nanopore system, the structure is simple; it is not susceptible to fouling and can be used multiple times.
Abreviaturas
- 3-APTES:
-
(3-Aminopropyl)triethoxysilane
- ABTS:
-
3-ethylbenzothiazoline-6-sulfonic acid
- EDC:
-
N-(3-dimethylaminopropyl)-N’-ethylcarbodiimide
- FIB:
-
Focused ion beam
- HRP:
-
Horseradish peroxidase
- KCl:
-
Potassium chloride
- NHS:
-
N-hydroxysuccinimide
- SEM:
-
Microscopía electrónica de barrido
- SNR:
-
Signal to noise ratio
Nanomateriales
- LiDAR de estado sólido ofrece una solución de detección automotriz más simple
- Nanosilicio para producir hidrógeno
- Los nanocristales semiconductores ayudan a producir combustible de hidrógeno
- Nano grafema, memoria transparente flexible basada en silicio
- Nanodots de carbono como nanosensores de modo dual para la detección selectiva de peróxido de hidrógeno
- Detección de peróxido de hidrógeno basada en la modificación de superficies internas de nanoporo de estado sólido
- Sensor plasmónico basado en nanoprismas dieléctricos
- Estimación del almacenamiento de energía del supercondensador basada en ecuaciones diferenciales fraccionales
- Nanopore de estado sólido
- Modificación del cocatalizador de aleación de PtNi del híbrido g-C3N4 / GO sensibilizado con eosina Y para una evolución eficiente del hidrógeno fotocatalítico de luz visible
- Ambarella, Lumentum y ON Semiconductor colaboran en la detección 3D basada en procesamiento de IA para dispositivos AIoT de próxima generación



