Introducción selectiva de impureza de Cu en ZnS finamente disperso obtenido durante el proceso de síntesis en una etapa
Resumen
Se investigó ZnS:Cu fino, obtenido mediante el método de síntesis autopropagable a alta temperatura. Como se utilizó el fundente en la mezcla NaCl, se tomaron Zn y S en relación estequiométrica; La concentración de Cu a cargo consistió en ~ 1,5% en peso. Utilizando datos de SEM, se estableció que el ZnS obtenido:Cu consta de dos fracciones, primero con tamaños de partículas de ~ 10 μm y más, y otro con tamaños de 50 a 500 nm. Se estableció que la composición de las fracciones de ZnS:Cu era esencialmente diferente. Según los datos de EDS, la concentración de Cu en partículas de fracción con tamaños de 50 a 500 nm consiste en ~ 2% en peso, y en partículas con tamaños de ~ 10 μm y más no se detectó la presencia de Cu. Se discuten las razones que conducen al dopaje selectivo de partículas en función de su tamaño y también el papel del NaCl en los procesos que se experimentan durante la síntesis de material.
Antecedentes
En la actualidad, se dedica una atención considerable al desarrollo de diferentes métodos tecnológicos nuevos de fabricación de estructuras de semiconductores complejos. En este sentido, son de especial interés las investigaciones relativas a la optimización de métodos de síntesis de materiales semiconductores dirigidos a la fabricación de estructuras semiconductoras de alta calidad (estequiométricas, sin impurezas, etc.) o complejas (soluciones sólidas, materiales nanoestructurados) en un ciclo tecnológico. Tales investigaciones también tienen importancia para el conocimiento fundamental porque permiten comprender más profundamente la interconexión entre estructura, composición y propiedades del material producido y los regímenes tecnológicos de su síntesis. Los estudios de regularidad de la interconexión mencionada anteriormente son importantes también en lo que respecta a las posibilidades de aplicación, la comprensión de las regularidades en la secuencia «composición - estructura - propiedades» permite controlar o modificar la estructura y propiedades de los materiales.
Un lugar particular en las investigaciones de la influencia del régimen de fabricación sobre la estructura y las propiedades de los materiales tiene el caso cuando se utilizan agentes de fusión en la síntesis de material. Si es necesario obtener la sustancia en forma de cristales bien formados, los fundentes se utilizan a menudo como mineralizadores. Es especialmente conveniente en las condiciones de alta temperatura cuando la alta movilidad de los átomos que forman la red puede conducir a la formación de una gran cantidad de defectos [1].
En este sentido, es interesante investigar las peculiaridades de la posibilidad de fabricación de ZnS obtenidas por el método de síntesis autopropagable a alta temperatura (SHS) utilizando como material fundente con enlace iónico. Las posibilidades tecnológicas de SHS son amplias y permiten realizar el dopaje de material por diferentes elementos y compuestos durante el proceso de síntesis. La variación de los métodos de proceso de combustión en la onda SHS brindan la posibilidad de fabricar un producto específico en forma de muestra fundida con tamaños preestablecidos, así como en forma de polvo con la dispersión de tamaño necesaria.
Es necesario señalar que el uso de fundentes permite controlar la temperatura del proceso de combustión y cambiar las condiciones de solubilidad del dopante en el material sintetizado. En particular, para proporcionar las condiciones para la denominada «solubilidad retrógrada» [2], cuando se introduce una impureza, o ingresa solo en áreas particulares del material o no ingresa en absoluto. Tal situación se realiza cuando el nivel de Fermi se cruza con la parte superior de la banda de estados de impureza localizados.
La variación de los métodos de proceso de combustión en la onda SHS brindan la posibilidad de fabricar un producto específico en forma de muestra fundida con tamaños preestablecidos, así como en forma de polvo con la dispersión de tamaño necesaria.
Este fenómeno será más pronunciado en materiales con bandas de estado de impurezas localizadas localizadas en máxima proximidad al nivel de Fermi. Dichos materiales se equilibran en el borde de estabilidad de los complejos covalentes del metal introducido y principal [3].
Este trabajo se dedicó a la clarificación de la influencia del NaCl introducido en la mezcla como agente de fusión, sobre la concentración de Cu en partículas de ZnS:Cu de dispersión fina de diferentes tamaños, obtenidas por el método SHS [4, 5].
Métodos
En el presente trabajo se realizaron investigaciones de ZnS:Cu fino obtenido por el método SHS (ZnS:Cu – SHS). Para la fabricación de ZnS:Cu – SHS, Zn y S se tomaron en relación estequiométrica. El dopado por mezcla de cobre se llevó a cabo a partir de cloruro de cobre CuCl directamente durante el proceso de síntesis. La concentración de Cu a cargo fue de ~ 1,5% en peso. ZnS:Cu se obtuvo a temperaturas que proporcionaron un proceso de interacción de azufre y zinc. Parte de la liberación durante la reacción de interacción de S y Zn fue absorbida por el fundente (NaCl), que permite disminuir la temperatura de síntesis del material. La cantidad de NaCl en la mezcla fue del 5% en peso.
Los espectros de fotoluminiscencia (PL) y los espectros de excitación luminiscente (PLE) se registraron a temperatura ambiente utilizando una instalación SDL-2. Durante el registro PLE, la excitación se llevó a cabo utilizando radiación de lámpara de xenón y monocromador MDR-12.
Los estudios de morfología y tamaño de partículas se llevaron a cabo utilizando un microscopio electrónico de barrido JAMP-9500F (Jeol).
Las mediciones de la composición de los elementos de las partículas se realizaron mediante el método de espectroscopía de rayos X de dispersión de energía (EDS) y el espectrómetro INCA PentaFETx3 (Oxford Instruments).
Resultados y discusión
Las imágenes típicas de SEM para fracciones finas después del enjuague en agua destilada se presentan en la Fig. 1. Como se ve en las imágenes de SEM, la fracción fina sintetizada representa a sí misma una mezcla de partículas con diferentes tamaños, en las que están presentes nanopartículas y también partículas de tamaños micro y submicrónicos. .

Imágenes SEM de ZnS:Cu fino, obtenidas por el método SHS. un Vista general. b Partículas de mezcla de diferentes tamaños
En la Fig. 2, se presentan los espectros PL y PLE de ZnS – SHS. Como se ve en la Fig. 2, el espectro PL de ZnS – SHS, representa a sí mismo una banda ancha con un máximo en la región de 505–525 nm. Es bien sabido que la banda PL de ZnS:Cu en la región azul-verde es compleja y, como es habitual, representa en sí misma la superposición de varias bandas, que están determinadas por la mezcla de cobre y también por defectos intrínsecos de ZnS. La naturaleza de los centros de luminiscencia, que determinan las bandas azul y verde de Cu en ZnS, se describe en detalle en [6, 7, 8]. Los autores de [6, 7, 9,10,11,12,13] han mostrado, ese centro, que es responsable de la aparición de la banda verde de Cu con λ max ~ 505 ÷ 530 nm, es ión de cobre aislado, que sustituye al ión de zinc en la red de ZnS.
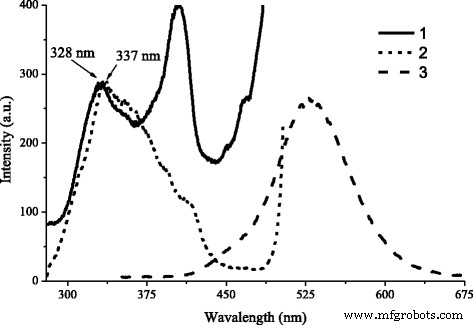
Espectros PLE de ZnS:Cu sintetizados por SHS, normalizados en la banda de absorción fundamental de intensidad. 1 - ZnS inicial:Cu - SHS, 2 - ZnS:Cu - SHS después del lavado en agua destilada. 3 - Espectro PL de ZnS inicial:Cu - SHS
Banda azul con λ max ~ 440 ÷ 465 nm se conectan con la formación de asociados similares al tipo de par DA Cu i -Cu Zn [6, 7, 13] o Cu Zn - Cu Zn [11, 12]. En la región espectral dada, también están presentes las bandas que son causadas por centros de oxígeno [6, 10, 14] y bandas de radiación autoactivada de [6, 7, 11, 12].
PLE de ZnS:Cu – SHS (Fig. 2, curva 1) incluye bandas correspondientes a las transiciones de excitación de banda a banda en ZnS en masa y de tamaño cuántico. Esto indica la presencia en el material de partículas grandes con tamaños superiores a cientos de nm y también de partículas con tamaños inferiores a 5 nm (es decir, radio de excitón de Bohr en ZnS). Según [14], E g El valor de ZnS consiste en ~ 3,65 eV, que corresponde a la banda de absorción de 340 nm. El desplazamiento del máximo de la banda de absorción fundamental en 10 nm, indica la presencia en el material de las partículas con tamaños correspondientes a la manifestación del efecto de tamaño cuántico [15].
Después de lavar el material inicial en agua destilada, el máximo de absorción fundamental se desplazó hacia el lado de onda larga (Fig. 2, curva 2). Esto atestigua que el lavado en agua destilada ha conducido no solo a la erosión del material de NaCl que quedó después de la síntesis, sino también a las partículas con tamaños inferiores a 5 nm.
Según los datos de la microscopía electrónica de barrido (ver Fig. 1), la parte principal del material obtenido consta de dos fracciones aisladas. La primera fracción consta de partículas individuales con tamaños de ~ 10 μm (Fig. 1a). La segunda parte está representada por partículas con tamaños desde cientos de nanómetros hasta varios micrones (Fig. 1b).
Así, la composición elegida de regímenes de carga y síntesis permitió obtener simultáneamente, es decir, durante una síntesis, las partículas con nano, meso y micro tamaño.
Las investigaciones de la composición del elemento por EDS han demostrado que en ZnS:Cu obtenido en diferentes partículas la violación de la estequiometría puede consistir en hasta 4 at. % (Tabla 1).
Al mismo tiempo, de acuerdo con los datos de estas investigaciones, la presencia de dopante de cobre en partículas con tamaños del orden de cientos de nm es del orden de ~ 2% en peso (Figs. 3a, 2), y en partículas grandes con tamaños ~ 10 μm no se detectó la presencia de Cu (Figs. 3a, 1). En la Tabla 1, se presenta la composición de elementos (en% at.) De partículas en conglomerados y de partículas grandes separadas que se muestran en la Fig. 1a.
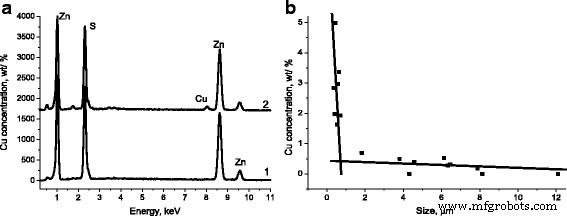
un Espectros EDS de partículas de ZnS – SHS con tamaños:1–27 μm, 2–0,3 μm. b Concentración de Cu en dependencia de los tamaños de partículas de ZnS-SHS
En la Fig. 3b se muestra la concentración de Cu en dependencia de los tamaños de partículas de ZnS-SHS. Como se ve en la Fig. 3b, para partículas con tamaños de ~ 300 hasta ~ 700 nm anomalía se observa una alta concentración de dopante de cobre, con un valor de ~ 5% en peso para partículas de tamaño de 370 nm. Al mismo tiempo, para partículas con tamaños de ~ 2 hasta 12 μm, la concentración de cobre no es superior al 0,7% en peso, y en algunas partículas (con tamaños de ~ 8 μm, ~ 12 μm), el dopante de cobre no está registrado por el método EDS, es decir, está prácticamente ausente. Es necesario señalar aquí que la concentración de cobre a cargo consistió en ~ 1,5% en peso. Así, como atestiguan los datos mencionados anteriormente, el dopaje por cobre de las partículas de ZnS, que se forman durante el proceso de síntesis, se realiza de diferente manera dependiendo de sus tamaños.
Consideremos las razones que pueden explicar un nivel de dopaje tan bajo para partículas grandes (2 ÷ 12) y un nivel de dopaje extremadamente alto para partículas pequeñas (<2 μm) de ZnS:Cu - SHS.
En nuestro caso, la formación de ZnS (materiales con enlace iónico-covalente, porcentaje de enlace iónico ~ 40% [15]) se realiza con vecindad próxima con NaCl (material iónico [16]. La aparición de la fase de ZnS durante el proceso de síntesis se somete a liberación de calor , que en su caso conduce a la descomposición del CuCl en los componentes y la fusión del NaCl. Temperatura de fusión del NaCl - 800 ° C, temperatura de ebullición - 1465 ° C [17]. La descomposición del CuCl en los componentes se somete a una reacción de desproporción, que conduce a la formación de CuCl 2 con liberación de Cu a 500 ° C [18], y con un aumento de temperatura superior a 500 ° C, CuCl 2 en su caso se descompone en CuCl y Cl con posterior volatilización del Cl. Es decir, la cristalización de ZnS se somete a la fusión de la mezcla de NaCl y ZnS. Este tipo de procesos durante el transporte en sistemas sólido-líquido se denominan mineralización [1, 19].
Así, la formación de partículas de ZnS de diferentes tamaños se produce en paralelo. Las partículas grandes de ZnS se forman en estado fundido o en el entorno de NaCl. El transporte de cobre a través de la fase líquida de NaCl es difícil debido a su baja solubilidad [20], además de eso, la descomposición de CuCl no se produce de una sola vez, y eso también reduce la tasa de introducción de Cu en ZnS.
La formación de partículas de pequeño tamaño, muy probablemente, se realiza en fase gaseosa de Zn y S. En este caso, la aparición de la fase CuS tiene baja probabilidad, porque para su formación se necesita mayor cantidad si se necesita calor [20]. Después de la formación, las partículas pequeñas están próximas al Cu y las partículas grandes de ZnS. Debido a que el tamaño de las partículas pequeñas se vuelve proporcional al tamaño de la región de carga espacial (SCR) en ZnS, entonces las partículas están en la región de agotamiento del portador de carga. Esto se debe al hecho de que cuando el tamaño de las partículas disminuye hasta un valor menor que el doble del valor de la profundidad de cribado ( L ) se produce la imposición de SCR localizado a lo largo de una superficie de partícula en el SCR de la superficie opuesta. La superposición mutua de superficies SCR conduce a una disminución del ancho entre el nivel de Fermi E F y la parte superior de la banda de valencia E V [21]. En consecuencia, la concentración de los principales portadores de carga en partículas de tamaño r < 2 L resulta bajo, o en otras palabras, la partícula resulta en la zona de agotamiento. En este caso, como se menciona en [3], cuando la banda de impurezas se llena más de la mitad, la transición de fase de primer orden, acompañada de un cambio brusco del valor del potencial químico y otros parámetros termodinámicos del material, es termodinámicamente favorable. En caso contrario, la transición se acompaña del aumento del nivel de Fermi durante el calentamiento, que corresponde a la entropía negativa del proceso, es decir, se debe observar la descomposición del material homogéneo en las regiones enriquecidas con portadores a una concentración que asegure el llenado de la banda de impurezas. no menos de la mitad y en regiones agotadas por los transportistas. Es decir, el descenso del nivel de Fermi y su entrada en la zona de niveles de impurezas conduce a su vaciado, que es termodinámicamente desfavorable para el material. En consecuencia, la introducción de cobre como impureza donante en ZnS, donde el cobre ocupa una posición intersticial se vuelve termodinámicamente favorable para el material. Posiblemente esto haya llevado a una concentración tan alta de cobre en las partículas de fracción pequeña. Además, para una interpretación más inequívoca de los resultados obtenidos, las investigaciones adicionales son necesarias.
Por lo tanto, los resultados presentados muestran que el método SHS permite obtener materiales con tamaños de partículas de ZnS en un amplio rango, desde micro hasta nano tamaños. Además de eso, la elección de los regímenes de síntesis, el material fundente y su cantidad en la mezcla permite dopar selectivamente las partículas en función de sus tamaños.
Conclusiones
Las investigaciones realizadas de ZnS:Cu obtenido por el método SHS con adición de NaCl a cargo como fundente han demostrado que la introducción de NaCl permite incrementar la cantidad de fracción fina (50-500 nm) en el material. Los datos de EDS han demostrado que la concentración de Cu en fracciones es diferente. La concentración de Cu en la fracción con tamaños de partículas entre 50 y 500 nm consiste en ~ 2% en peso, y en partículas con tamaños de ~ 10 μm y más, no se detectó la presencia de Cu. Por lo tanto, la selección de los regímenes de síntesis, el material de flujo y su cantidad a cargo permite, cuando se usa el método SHS, realizar el dopaje selectivo de partículas en función de su tamaño. Los resultados obtenidos están bien explicados dentro de los marcos del modelo de «solubilidad retrógrada» de impurezas en materiales multicomponente.
Abreviaturas
- CuCl :
-
Cloruro de cobre
- NaCl :
-
Cloruro de sodio
- SHS :
-
Síntesis autopropagable a alta temperatura
- ZnS :
-
Cu ZnS dopado por Cu
- ZnS :
-
Cu – SHS -ZnS:Cu obtenido por método SHS
- ZnS :
-
Sulfuro de zinc
Nanomateriales
- Introducción a las partes de un cerrojo
- En el campo de las plantas de proceso con Ethernet
- Introducción a la banda de terahercios
- Introducción al proceso de infusión de resina
- Introducción a la soldadura ultrasónica de plásticos
- Cómo funciona el proceso de CMC
- ¿Qué hay en el proceso de fabricación?
- Una mirada al proceso de tasación de equipos usados:cómo funciona
- ¿Cuál es el proceso de fabricación del jabón?
- Introducción al proceso de fundición a la cera perdida de acero inoxidable
- Simplificación del proceso



