Diagrama de equilibrio de carbono de hierro con explicación [Diagrama de fase]
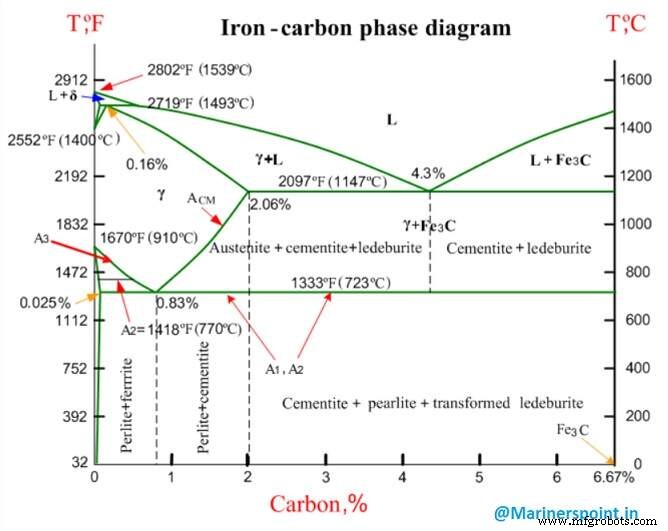
En este artículo discutiremos sobre el Diagrama de equilibrio de hierro y carbono , usos del diagrama de equilibrio, tipos de diagrama de equilibrio de carbono de hierro y varias fases y términos asociados con el diagrama de fase de carbono de hierro.
¿Qué son los diagramas de fase?
Diagramas de fase son representaciones gráficas de las fases presentes en una aleación bajo diversas condiciones de temperatura, presión y composición química.
La solidificación de las aleaciones metálicas se entiende claramente por medio de diagramas de equilibrio. Estas son representaciones gráficas de cambios de estado debido a variaciones de temperatura y concentración. Dado que este diagrama indica la naturaleza y constitución de las aleaciones, y la cantidad y composición de las fases en un sistema dado, también se le conoce como diagrama de constitución o diagrama de fase.
Características y usos del diagrama de equilibrio
Equilibrio Implica que los cambios que ocurren en un sistema como resultado de que el proceso avance en una dirección son totalmente compensados por los cambios debidos a la inversión del proceso en el sistema. Por lo que se considera como una condición dinámica de equilibrio entre movimientos atómicos donde la resultante es cero.
Las tasas de cambios de temperatura o de composición han sido extremadamente lentas durante el trabajo experimental, por lo que la aleación "se detendría" antes de que una variable como la temperatura volviera a cambiar. La condición, por lo tanto, es de descanso más que de cambio.
El diagrama de equilibrio indica lo siguiente:
2. Posibles cambios de fase que se producirán como consecuencia de la alteración de la composición o temperatura.
¿Qué representa el diagrama de equilibrio?
El diagrama describe las condiciones adecuadas para que existan dos o más fases en equilibrio. Por ejemplo, el diagrama de fases del agua describe un punto (punto triple) donde el agua puede coexistir en tres fases diferentes al mismo tiempo. Esto sucede justo por encima de la temperatura de congelación (0,01 °C) y 0,006 atm.
Usos del diagrama de equilibrio en metalurgia
- Desarrollo de las nuevas aleaciones sobre la base de los requisitos de la aplicación.
- Producción de estas aleaciones.
- Desarrollo e implementación de procedimientos de tratamiento térmico adecuados para mejorar las propiedades químicas, físicas y mecánicas de estas nuevas aleaciones.
- Solucionar problemas que surgen durante el uso de estas nuevas aleaciones, lo que finalmente mejora la previsibilidad del producto.
Diagrama de equilibrio de hierro y carbono
El diagrama de equilibrio de hierro y carbono (también llamado diagrama de fase de carbono de hierro) es una representación gráfica de los respectivos estados de microestructura de la aleación de hierro-carbono (Fe-C) según la temperatura y el contenido de carbono.
El diagrama de fase de carbono de hierro se usa comúnmente para comprender completamente las diversas fases del acero y el hierro fundido. El acero y el hierro fundido son aleaciones de hierro y carbono. Además, ambas aleaciones contienen oligoelementos en pequeñas cantidades.
El gráfico es bastante complejo, pero debido a que estamos limitando nuestra investigación a Fe3C, solo veremos hasta un 6,67 por ciento en peso de carbono.
Tipos de diagrama de equilibrio de hierro y carbono
El diagrama de equilibrio de carbono de hierro binario es la base del acero y el hierro fundido. Se trata de transformaciones que ocurren en aleaciones que tienen composiciones de hierro puro a cementita (6,67 por ciento de carbono). Hay dos versiones del diagrama de equilibrio de carbono de hierro:
Estos dos sistemas dependen de la velocidad de enfriamiento. El enfriamiento rápido produce cementita y el sistema se conoce como sistema hierro-cementita . En este sistema, las estructuras formadas en las fases solidificadas no alcanzan un equilibrio suficientemente completo. Entonces el sistema hierro-cementita es un metaestable uno.
Mientras que el enfriamiento lento produce grafito y el sistema es conocido como sistema Hierro-grafito . Las estructuras que se forman en la fase solidificada alcanzan un equilibrio suficientemente completo. Así que este es un estable una.
Tipos de aleaciones ferrosas en diagrama de equilibrio de carbono-hierro
La escala de porcentaje de peso en el eje X del diagrama de fase de carbono de hierro oscila entre 0 % al 6,67 % Carbón. El metal se conoce simplemente como hierro o hierro puro hasta un contenido máximo de carbono de 0,008. porcentaje en peso de carbono. A temperatura ambiente, existe en la ferrita estado.
Acero es una aleación de hierro y carbono con un contenido de carbono que oscila entre 0,008 y 2,14 por ciento. Los grados de acero dentro de este rango se conocen como acero con bajo contenido de carbono. (o acero dulce), acero al carbono medio y acero con alto contenido de carbono .
Cuando el contenido de carbono supera 2,14 por ciento, llegamos al hierro fundido escenario. El hierro fundido es extremadamente duro, pero su fragilidad limita severamente sus aplicaciones y métodos de formación.
SISTEMA HIERRO-CEMENTITA
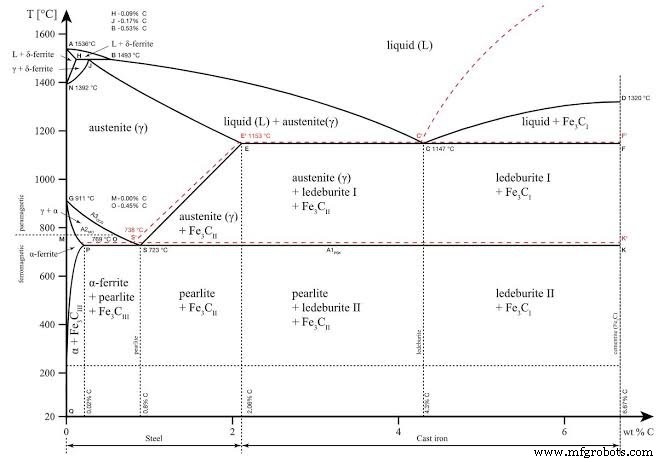
Si se elabora una serie de curvas de calentamiento tiempo-temperatura para aceros con diferentes contenidos de carbono y se trazan los puntos críticos correspondientes, se obtendrá un diagrama similar al de la figura 2.14. Este diagrama, que se aplica únicamente en condiciones de enfriamiento lento, se conoce como diagrama de fase hierro-carbono parcial. . Al consultar este diagrama, se pueden observar fácilmente las temperaturas de enfriamiento adecuadas para cualquier acero al carbono. Los puntos críticos de la figura 2.14 en la línea PSK se indican con A1, los de la línea GS con A3 y los de la línea SE con Acm. P>
Diagrama de equilibrio de hierro-carbono con explicación
Austenita
Austenita , solución sólida de carbono y otros constituyentes en una forma particular de hierro conocida como hierro γ (gamma). Tomemos el ejemplo de una pieza de acero al 0,20 % de carbono que se ha calentado a una temperatura de unos 850 °C. Por encima de Ar3, punto (línea GS) este acero es una solución sólida (tipo intersticial) de carbono en hierro gamma y se denomina austenita . Tiene una red cúbica centrada en las caras y no es magnética.
La austenita simple puede contener hasta un 2 por ciento de carbono a una temperatura de 1130°C. Al enfriar este acero, los átomos de hierro comienzan a formar una red cúbica centrada en el cuerpo debajo del punto Ar3 (línea GS). Esta nueva estructura que se está formando se llama ferrita o hierro alfa y es una solución sólida de carbono en hierro alfa que contiene hasta un 0,008 por ciento de carbono a temperatura ambiente.
A medida que el acero se enfría a Ar1 (línea PSK), se forma ferrita adicional. En la línea Arı, la austenita que queda se transforma en una nueva estructura llamada perlita. . El nombre de perlita se debe a su brillo nacarado. Consiste en placas alternas de ferrita y cementita y contiene alrededor del 87 por ciento de ferrita. La perlita puede tener una estructura laminar o granular de fina a gruesa. Esta es una sustancia fuerte y se puede cortar razonablemente bien con herramientas de corte, es decir, el componente de perlita en el acero es mecanizable.
Acero eutectoide
A medida que el contenido de carbono del acero aumenta por encima del 0,20 por ciento, la temperatura a la que la ferrita se rechaza por primera vez de la austenita cae hasta que, a aproximadamente el 0,80 por ciento de carbono (punto S), no se rechaza ninguna ferrita libre de la austenita. Este acero se llama acero eutectoide y es 100 por ciento perlita .
Eutectoide Punto
¿Qué es el Punto Eutectoide?
El punto eutectoide en cualquier metal, como se dijo antes, es la temperatura más baja a la que se producen cambios en una solución sólida.
Si el contenido de carbono del acero es superior al eutectoide (0,8 por ciento de carbono), se observa una nueva línea en el diagrama de fase de carbono del hierro indicado por Acm (línea S). La línea indica la temperatura a la que se rechaza por primera vez el carburo de hierro de la austenita en lugar de la ferrita.
El carburo de hierro (Fe3C) se conoce como cementita . Es extremadamente dura, quebradiza y se presenta como placas paralelas (capas lamelares), como partículas redondeadas (esferoides) o como envolturas alrededor de los granos de perlita. En el punto C, la mezcla eutéctica que contiene un 4,3 % de carbono se conoce como ledeburita. . Esto rara vez se ve en aleaciones enfriadas lentamente, ya que se descompone, debido a su naturaleza inestable, en otras fases durante el enfriamiento después de la solidificación.
Hipoeutectoide e hipereutectoide
Los aceros que contienen menos del 0,80 % de carbono se denominan hipoeutectoide. y las que contienen más del 0,8 por ciento de carbono se denominan hipereutectoides. aceros Esta terminología se aplica solo a los aceros simples y de baja aleación. Con los aceros de alta aleación se altera la composición eutectoide y la estructura puede incluso no existir.
En primer lugar, debe señalarse que el diagrama de equilibrio normal realmente representa el equilibrio metaestable entre el hierro y el carburo de hierro (cementita). La cementita es metaestable y el verdadero equilibrio debería estar entre el hierro y el grafito.
Aunque el grafito se encuentra ampliamente en los hierros fundidos (2-4% en peso de C), por lo general es difícil obtener esta fase de equilibrio en los aceros (0,03-1,5% en peso de C). Por lo tanto, se debe considerar el equilibrio metaestable entre el hierro y el carburo de hierro, ya que es relevante para el comportamiento de la mayoría de los aceros en la práctica.
Sistema de hierro y grafito
SISTEMA HIERRO-GRAFITO
Ya se ha dicho que el carburo de hierro o cementita es un metaestable, aunque en condiciones normales tiende a persistir indefinidamente. Cuando la cementita se descompone, lo hace de acuerdo con la reacción:
En la fase estable, carbono o grafito libres ocurre en lugar de la fase conocida como cementita . Tras un pequeño grado de sobreenfriamiento, se forma grafito cuando el hierro fundido se solidifica desde el estado líquido. El enfriamiento lento promueve la grafitización . El enfriamiento rápido suprime parcial o completamente la grafitización y conduce a la formación de cementita.
En la figura 2.14 se muestra un sistema de hierro y grafito (como línea de puntos). Se toma como ejemplo el caso de una aleación de carbono que contiene un 3,5 por ciento de carbono en peso.
En el punto 1 la aleación está en estado líquido. En el punto 2 de la línea de enfriamiento, la reacción que ocurre se puede expresar como:
Imagen
> Entre los puntos 2 y 3, el exceso de carbono en la austenita se precipita como grafito libre y no como cementita. En el punto 3 se produce la reacción eutectoide. Esto se expresa como:
Imagen
El mecanismo de transformación eutectoide debe transformar una única fase sólida en otras dos, ambas con composiciones diferentes a la original.
Tomando como ejemplo la descomposición eutectoide del hierro, la austenita que contiene 0,8% C se transforma en ferrita (hierro que casi no contiene carbono) y cementita (Fe3C, que contiene 25% at de carbono). Por lo tanto, los átomos de carbono deben difundirse juntos para formar Fe3C, dejando ferrita. Se forman núcleos de placas pequeñas de ferrita y cementita en los límites de grano de la austenita, y la difusión de carbono tiene lugar a una escala muy local justo delante de la interfase (esquema a continuación).
Así crecen las placas, consumiendo la austenita a medida que avanzan, para formar perlita. El proceso de grafitización se controla variando la velocidad de enfriamiento y la aleación adecuada de la matriz metálica.
Términos utilizados en el diagrama de equilibrio de hierro y carbono
Punto eutéctico
El punto eutectoide de cualquier metal es la temperatura más baja a la que se producen cambios en una solución sólida.
Las reacciones eutécticas ocurren en estos puntos, donde una fase líquida se congela en una mezcla de dos fases sólidas. Esto ocurre cuando una aleación líquida de composición eutéctica se enfría hasta su temperatura eutéctica.
Las aleaciones eutécticas son las aleaciones que se forman en este punto. Las aleaciones en los lados izquierdo y derecho de este punto se conocen como aleaciones hipoeutécticas y aleaciones hipereutécticas ("hipo" en griego significa menor que, "hiper" significa mayor que).
Austenita
Austenita, solución sólida de carbono y otros constituyentes en una forma particular de hierro conocida como hierro γ (gamma).
Esta fase es una solución sólida de carbono en FCC Fe con una solubilidad máxima de 2,14 % C. Al calentarse más, se convierte en ferrita BCC a 1395 °C. La γ-austenita es inestable a temperaturas por debajo de la temperatura eutéctica (727 °C) a menos que se enfríe rápidamente.
Alfa hierro o ferrita
Existente a bajas temperaturas y bajo contenido de carbono, la ferrita α es una solución sólida de carbono en BCC Fe. Esta fase es estable a temperatura ambiente. En el gráfico, se puede ver como una astilla en el borde izquierdo con el eje Y en el lado izquierdo y A2 en el derecho. Esta fase es magnética por debajo de 768°C.
Tiene un contenido máximo de carbono de 0,022 % y se transformará en γ-austenita a 912 °C como se muestra en el gráfico.
Cementita
La cementita, una fase metaestable de esta aleación con una composición fija de Fe3C, es una fase metaestable de esta aleación. A temperatura ambiente, se descompone muy lentamente en hierro y carbono (grafito).
Este tiempo de descomposición es largo y llevará mucho más tiempo que la vida útil de la aplicación a temperatura ambiente. Otros factores, como las altas temperaturas y la adición de ciertos elementos de aleación, pueden influir en esta descomposición al promover la formación de grafito.
La cementita es dura y quebradiza, lo que la hace ideal para el refuerzo de acero. Sus propiedades mecánicas están determinadas por su microestructura, que está determinada por cómo se mezcla con la ferrita.
Hemos tratado de cubrir todos los términos relacionados con el diagrama de fase de carbono de hierro, incluidas las diversas fases y términos utilizados en él para comprenderlo mejor. Espero que les haya gustado este artículo sobre diagrama de equilibrio hierro-carbono . Por favor, dé su opinión en el comentario a continuación.
Tecnología Industrial
- Circuito con un interruptor
- Impresión 3D con material de alta resistencia - Fibra de carbono compuesta-Nylon
- Bentley lanza Bentayga con las ruedas de fibra de carbono más grandes del mundo
- Dron de carreras con monocasco de fibra de carbono completamente cerrado
- Porsche los inicia joven con el cochecito de bebé de fibra de carbono
- Mecanizado por descarga eléctrica (EDM):Mecánica, principios de funcionamiento y circuitos (con diagrama)
- Fabricación de hierro por alto horno y emisiones de dióxido de carbono
- ¿Cuáles son las partes de una soldadura? - Explique con un diagrama
- ¿Qué es el diagrama de fase hierro-carbono?
- 11 tipos diferentes de procesos de soldadura con la ayuda del diagrama
- Diferentes tipos de operaciones de chapa con diagrama



