Nanomateriales para mejorar la medicina regenerativa
¿Quién no ha visto alguna vez una película en la que un ser humano puede regenerar su cuerpo tras recibir un disparo o una puñalada?
Un ejemplo famoso es el de la autocuración de Wolverine. Aunque todavía estamos lejos de lograr tal hazaña, a veces son precisamente estas fantasías las que impulsan los avances científicos, y quizás pronto podamos hacerlos realidad.
Un gran paso en esta dirección es la producción de tejidos artificiales para reemplazar los tejidos naturales que se han perdido o que ya no son funcionales, como una prótesis de titanio.
Sin embargo, para alcanzar el nivel de los personajes de Marvel en la regeneración de nuestros cuerpos, debemos mejorar y llevar nuestra tecnología al siguiente nivel; y parece que nos hemos puesto manos a la obra.
Los científicos han desarrollado una nueva estrategia que ayuda al cuerpo humano a regenerar sus propios tejidos mediante el uso de enfoques basados en nanomateriales para controlar el crecimiento de las células, la respuesta inmunitaria y la remodelación de los tejidos.
Este nuevo y apasionante campo de la ciencia se conoce como medicina regenerativa. .
¡Déjame contarte más sobre esto!
¿Qué tienen que ver los nanomateriales con la medicina regenerativa?
En uno de nuestros artículos anteriores Nanopartículas magnéticas avanzadas para la detección y el tratamiento del cáncer , vimos cómo cuando un material se contrae a dimensiones muy pequeñas, puede adquirir propiedades radicalmente diferentes. La ciencia está logrando, día a día, encontrar nuevas aplicaciones para estas propiedades nanotecnológicas.
Una de las grandes promesas de los nanomateriales es la capacidad de ‘modular’ la respuesta inmune uniéndolos a biomoléculas humanas (anticuerpos, citoquinas, hormonas, etc…).
Pero, ¿qué significa esta 'modulación'?
Control de la respuesta inmune
El sistema inmunológico es el ejército de nuestro cuerpo. Y como en cualquier ejército, los soldados no solo se utilizan para atacar y destruir, sino también como recursos de apoyo. Por ejemplo, el sistema inmunitario se ocupa de todo tipo de contingencias, como la renovación de tejidos después de sufrir una lesión, y ayuda a controlar los desequilibrios ambientales, eliminando toxinas del metabolismo o sustancias extrañas dañinas.
Este control, o modulación, está orquestado por un sinfín de biomoléculas (por ejemplo, citoquinas, interleucinas y hormonas) cuya concentración actúa como una señal a las células indicándoles cómo deben comportarse en cada momento.
Cuando usamos un material artificial en un paciente para cubrir una quemadura, por ejemplo, es deseable que finalmente se integre en el cuerpo del paciente. Concretamente, nos gustaría que las células del paciente colonizaran y crecieran en el nuevo material para que eventualmente sea reemplazado por el propio tejido del paciente.
Desafortunadamente, el sistema inmunológico a menudo reconoce el material como una entidad ajena a nuestro cuerpo e intenta aislarlo creando una pared a su alrededor compuesta por tejidos conectivos fibrosos a través de un proceso conocido como fibrosis. Este es un material pobre en células pero rico en moléculas (macromoléculas como el colágeno o la fibrina) que sostienen estructuralmente a las células. Tiene propiedades que son significativamente diferentes de las del tejido original. Muchos de ustedes reconocerían lo rígido que se siente un tejido cicatricial en comparación con la piel normal. Una cicatriz ubicada en una articulación puede incluso impedir su movimiento.
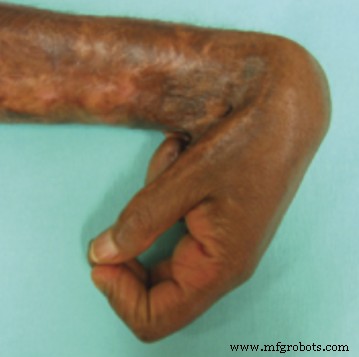
Figura 1 Formación de cicatrices hipertróficas con contractura articular Aarabi S, Longaker MT, Gurtner GC (2007) Formación de cicatrices hipertróficas después de quemaduras y traumatismos:nuevos enfoques para el tratamiento. PLoS Med 4(9):e234. doi:10.1371/journal.pmed.0040234 – http://www.plosmedicine.org/article/info%3Adoi%2F10.1371%2Fjournal.pmed.0040234
Destacado en mi artículo anterior Del PLA a la bioimpresión:herramientas de ciencia ficción para el campo médico , una estrategia para hacer frente a este rechazo por parte del sistema inmunitario es utilizar biomateriales para construir andamios (estructuras de apoyo para ser colonizadas por las propias células del paciente) a partir de moléculas, como el colágeno. Desgraciadamente, si implantamos un andamio compuesto únicamente por fibras de colágeno, el organismo acaba reabsorbiendo este material y, en el mejor de los casos, sustituyéndolo por fibrosis.
Esto nos puede interesar si queremos crear una “cicatriz artificial”, por ejemplo, para reparar la pared abdominal tras una hernia; en el que podríamos usar una malla Phasix™ hecha de poli-4-hidroxibutirato (P4HB) para reparar el defecto de la pared.
Para lograr la integración funcional de cualquier implante, debemos impulsar la diferenciación celular (es decir, dar a cada célula su tipo y función específicos) y evitar la posibilidad de que el sistema inmunitario rechace el implante. Podemos hacer esto mediante el uso de nanomateriales como "portadores" para entregar las biomoléculas y como señales para impulsar este proceso.
Pero, ¿y si pudiéramos inmovilizar o dirigir esas biomoléculas a cualquier lugar que queramos?
¿Podemos controlar el sistema inmunológico?
Por ejemplo, la combinación de nanomateriales y anticuerpos se puede utilizar para potenciar la respuesta inmunitaria, como en la lucha contra el cáncer (nanopartículas de óxido de hierro modificadas con anticuerpos).
Algunos nanomateriales ya tienen efectos inhibidores o estimulantes directos (dependiendo del material) sobre la respuesta inmune (metales nobles, nanopartículas de óxidos metálicos, óxido de cerio o dendrímeros son algunos ejemplos). Por lo tanto, simplemente recubriendo la superficie de un implante con esas nanopartículas, podemos detener un ataque del sistema inmunitario. [1]
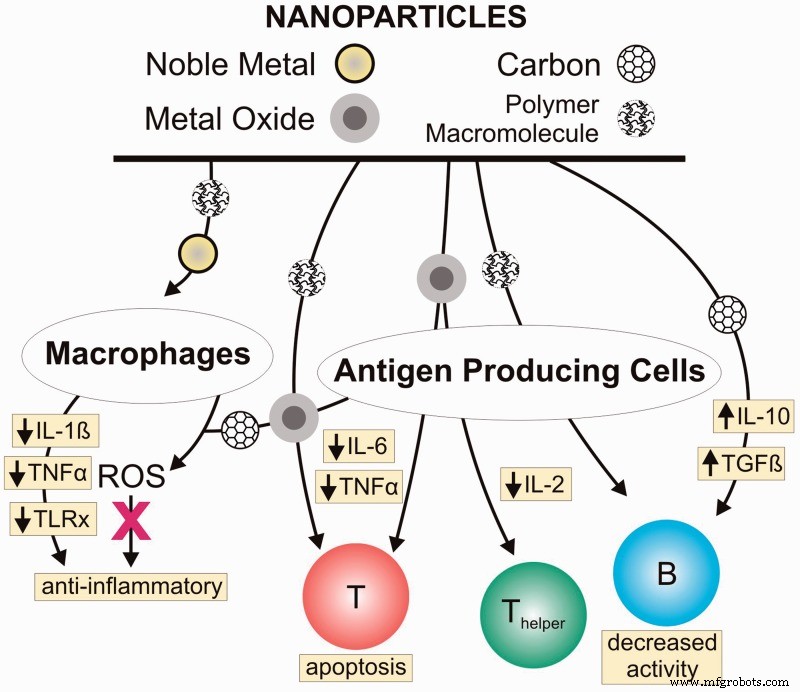
Figura 2 Nanomateriales con efectos inhibitorios directos sobre la respuesta inmune Ngobili Terrika A, Daniele Michael A. Nanoparticles and direct immunosuppression.1 Mayo, 2016 Experimental Biology and Medicine 106 Volumen:241 número:10, páginas:1064-1073; https://doi.org/10.1177/1535370216650053 https://journals.sagepub.com/doi/abs/10.1177/1535370216650053
Estrategias para inmovilizar nanomateriales y biomoléculas en superficies de implantes
Como ya hemos comentado, hay dos motivos principales para querer recubrir la superficie de un implante:o bien para aumentar su biocompatibilidad (para evitar que el sistema inmunitario lo ataque) o para fijar biomoléculas que estimulen y dirijan la proliferación celular (para sustituir la implante con tejido del propio paciente).
La idea de implantar un andamio biodegradable (recubierto con factores de crecimiento) para ser reemplazado con el tiempo por el tejido del paciente es un tema que ya discutimos en Del PLA a la bioimpresión:herramientas de ciencia ficción para el campo médico . Dichos andamios aún se encuentran en la fase de investigación, pero es solo cuestión de años antes de que potencialmente comencemos a verlos entrar en la práctica clínica.

Aumentar la biocompatibilidad de materiales extraños es una necesidad actual para la industria. Para asegurarnos de que el cuerpo humano no rechace un biomaterial implantado, tenemos que adherir a la superficie de nuestro implante el recubrimiento (nanomateriales o complejos biomolécula-nanomaterial) que regula el sistema inmunitario. Así, cuando una célula del sistema inmunitario se acerca demasiado a ella, el recubrimiento inhibe la célula y evita que se genere una reacción inflamatoria alrededor del implante.
¿Pero cómo podemos hacer tal recubrimiento?
Básicamente, hay dos formas de 'pegar' el recubrimiento a un implante:inmovilización no covalente e inmovilización covalente.
Inmovilización no covalente (NCI):
NCI es la estrategia más simple y económica para recubrir el implante, pero depende en gran medida de cuán hidrofílico sea el material del implante. Se basa en las cargas electrostáticas que generarían una fuerza de atracción entre el material que estamos implantando y el revestimiento.
Este método proporciona una liberación rápida de biomoléculas, por lo que es más conveniente cuando estamos interesados en una respuesta abrupta pero de corta duración. Su mayor ventaja, además, es su bajo coste de fabricación.
El NCI se puede aplicar por adsorción (partículas diminutas de tamaños entre 500 y 1 mm que se adhieren a la superficie) o atrapamiento (partículas atrapadas en una matriz porosa). [2]
En el atrapamiento, la matriz está hecha con polímeros solubles en agua como carragenina, colágeno parcialmente hidrolizado (gelatina), alginato, agar o triacetato de celulosa.[2, 3]
Pero, ¿qué sucede cuando el material del implante es hidrófilo y la biomolécula es hidrófoba (o viceversa)?
Una idea simple puede ser una solución efectiva:¡encapsulación de la biomolécula!

Encapsulación en el recinto de la biomolécula, que puede llevarse a cabo fácilmente utilizando polímeros, como agarosa, poli(etilenglicol) (PEG) o poli(N-vinilpirrolidona) (PVP).
Un ejemplo de este método es el uso de un andamio de polisulfona relleno con una solución de gel de agarosa infundida con biomoléculas para guiar la regeneración de las fibras nerviosas y reducir la inflamación [4].
Además, si el andamio no es del todo hidrofílico, la mejor estrategia para inmovilizar la biomolécula es encapsularla en una fase acuosa separada a través de un proceso llamado agua en aceite en agua (o doble emulsión). También podemos realizar la absorción directa sobre la superficie del material mediante disolventes orgánicos.
Un ejemplo de un polímero hidrófobo ampliamente utilizado para inmovilizar biomoléculas como factores hormonales o incluso fármacos es el poli(ácido láctico-co-glicólico) (PLGA).
Inmovilización covalente (IC)
La inmovilización covalente consiste en crear un enlace irreversible entre nuestras biomoléculas específicas y el polímero del que está hecho nuestro implante mediante lo que llamamos agentes reticulantes; son compuestos químicos que reaccionan ante una condición física (calor, luz…) y nos ayudan a crear un vínculo que podría enlazar, por ejemplo, una cadena polimérica con otra (podríamos imaginarlos como grilletes que se cierran con luz o calor para unir ambos polímeros).
Este método conduce a un efecto mucho menos abrupto sobre el sistema inmunológico, aunque es mucho más duradero; de ahí que sea preferible utilizarlo cuando estemos interesados en una respuesta estable y a largo plazo.
La principal ventaja de este método es que nos permite realizar la diferenciación de tejidos estratificados. Esto significa que podemos diseñar diferentes puntos de unión en nuestro andamio para diferentes factores, creando así regiones con diferentes concentraciones de biomoléculas para promover un tejido estructurado diferencialmente.
Como elemento base se pueden utilizar andamios de colágeno-glicosaminoglicano (CG) (utilizando carbodiimida como reticulante dada la ubicuidad de los grupos NH2 en su superficie).
Un ejemplo de inmovilización covalente sería la conjugación de polietilenimina (PEI) con heparina para crear una cubierta con el fin de aumentar la biocompatibilidad de las superficies de aleación de NiTi [5].
Un método de entrecruzamiento que está cobrando importancia en los últimos años es el uso de acrilatos para polimerizar hidrogeles de PEG. Los acrilatos son grupos funcionales sensibles a la luz ultravioleta. Estos grupos se pueden agregar a péptidos (u otros factores de crecimiento), guiando así la síntesis por fotopolimerización de andamios compuestos por híbridos de polímero y biomolécula. La posibilidad de integrar este proceso con la impresión 3D para dar un patrón estructural a nuestro andamio está convirtiendo a la fotopolimerización en uno de los métodos más relevantes para inmovilizar biomoléculas.
También se han diseñado procesos de fotolitografía alternativos, por ejemplo, el Instituto Fraunhofer de Ingeniería Interfacial y Biotecnología utiliza un método que consiste en unir factores de crecimiento a andamios CG usando benzofenona (BP). [6, 7]
Otra diana más selectiva, por su menor ubicuidad respecto al grupo NH2, es el grupo SH. Los reticuladores a base de sulfhidrilo se utilizan ampliamente para crear un recubrimiento que inhibe la activación del complemento (un componente muy importante del sistema inmunitario) contra nuestro injerto [8].
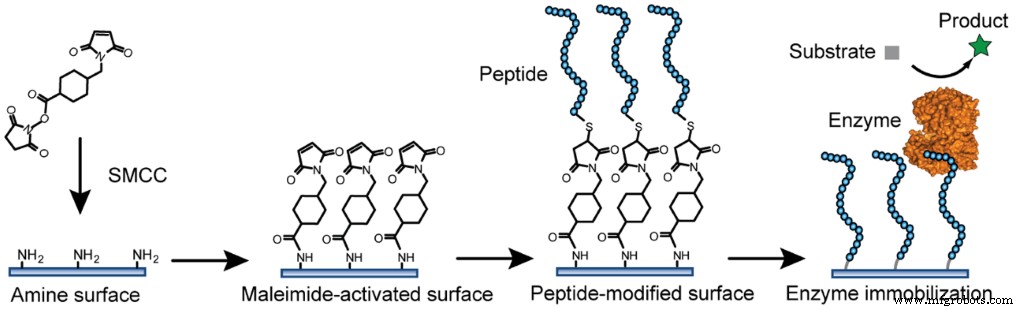
Figura 3 Ejemplo de inmovilización de enzimas mediante unión covalente Fu J, Reinhold J, Woodbury NW (2011) Superficies modificadas con péptidos para la inmovilización de enzimas. PLoS ONE 6(4):e18692. https://doi.org/10.1371/journal.pone.0018692 https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0018692
Conclusiones
Entonces, claramente existen diferentes estrategias para inmovilizar biomoléculas en la superficie de un material para controlar la respuesta inmune o el proceso de diferenciación.
Antes de elegir un método de inmovilización, es importante conocer las propiedades del material que va a utilizar y la curva del perfil de liberación de biomoléculas que desea lograr. El mejor enfoque es una combinación de diferentes métodos de conjugación, teniendo en cuenta que el sistema inmunológico no tiene una naturaleza estática. Muestra una variación dinámica a lo largo del tiempo.
El recubrimiento de implantes utilizando nanomateriales (o complejos nanomateriales-biomolécula) para aumentar la biocompatibilidad de los implantes es ampliamente utilizado en la actualidad. Sin embargo, este hecho contrasta fuertemente con el caso de la fabricación de andamios con una concentración estratificada de biomoléculas encapsuladas o unidas. A pesar de la enorme cantidad de actividad en este campo, hoy en día no hay muchas empresas que proporcionen estos andamios, y aún quedan muchas acciones regulatorias por abordar antes de lanzar estos productos al mercado.
Eso significa que tendremos que esperar un poco más para poder realizar una curación completa sin cicatrices. Pero la espera, muy probablemente, no será larga. Esta tecnología prometedora bien puede usarse en la práctica médica diaria en unos pocos años.
Tecnología Industrial
- Cómo las escaleras mejoran la seguridad y la confiabilidad
- El grafeno pone los nanomateriales en su lugar
- Cómo la IA mejorará los entornos de IoT
- La red neuronal artificial puede mejorar la comunicación inalámbrica
- Las claves de cifrado biológico pueden mejorar los niveles de seguridad en la era post cuántica
- Mejore la colaboración interfuncional con comunidades de práctica
- Principios básicos de los accionamientos regenerativos:Parte 2
- El valor del corte por chorro de agua en medicina
- 5 aplicaciones del mundo real de la IA en medicina (con ejemplos)
- Mejore el conocimiento operativo de su empresa
- Fabricación aditiva en medicina y odontología



