Nanohojas V6O13 interconectadas en 3D cultivadas en textiles carbonizados a través de un proceso hidrotermal asistido por semillas como cátodos flexibles de alto rendimiento para baterías de iones de litio
Resumen
Se ha demostrado que los materiales nanoestructurados independientes tridimensionales (3D) son uno de los electrodos más prometedores para el almacenamiento de energía debido a su rendimiento electroquímico mejorado. Y también se estudian ampliamente para los sistemas de almacenamiento de energía portátiles. En este trabajo, V 6 interconectado O 13 Las nanohojas se cultivaron en el tejido carbonizado flexible (c-textile) mediante un método hidrotermal asistido por semillas para formar un electrodo 3D autónomo para baterías de iones de litio (LIB). El electrodo exhibió una capacidad específica de 170 mA h g −1 a una corriente específica de 300 mA g −1 . Con el recubrimiento de nanotubos de carbono (CNT), sus capacidades específicas aumentaron aún más entre un 12% y un 40% a las distintas tasas actuales. Podría retener una capacidad reversible de 130 mA h g −1 , 74% de la capacidad inicial después de 300 ciclos a la corriente específica de 300 mA g −1 . Superó a la mayoría de los óxidos de vanadio de valencia mixta. El rendimiento electroquímico mejorado se atribuyó al efecto sinérgico de la nanoestructura 3D de V 6 O 13 para Li + factible Difusión y transporte y red conductora jerárquica altamente conductora formada por CNT y fibra de carbono en c-textil.
Antecedentes
Óxidos de vanadio (p. Ej., V 6 O 13 , V 3 O 7 , V 2 O 5 ) son materiales catódicos aplicables para baterías de iones de litio (LIB) de alta energía, debido a su bajo costo, altas capacidades específicas y la abundancia de elementos de vanadio [1,2,3,4,5,6]. Entre los óxidos, V 6 O 13 ha sido considerado como un excelente candidato del material del cátodo [7,8,9,10,11,12,13,14]. Su capacidad teórica y densidad de energía pueden alcanzar 417 mA h g −1 y 890 Wh kg −1 cuando se litiga en el producto final, Li 8 V 6 O 13 [2, 8]. Sin embargo, V 6 O 13 Los electrodos han sufrido un ciclo de vida corto y una capacidad de baja velocidad durante mucho tiempo porque V 6 O 13 La conductividad electrónica disminuye cuando se procesa mientras Li + coeficientes de difusión (10 −8 a 10 −9 cm 2 S −1 ) son bajos [7, 9]. La construcción de nanoestructuras 3D independientes es un método eficaz para resolver los problemas anteriores. La nanoestructura 3D puede mejorar el transporte / difusión de iones / electrones al tiempo que evita eficazmente la autoagregación [15,16,17,18,19,20]. Por ejemplo, Yu et al. 3D V 6 sintetizado O 13 nanotextiles ensamblados a partir de nanohorros interconectados a través de una ruta fácil de autoensamblaje basada en soluciones redox con MnO 2 plantilla a temperatura ambiente. En un rango de voltaje de 1 a 4 V, V 6 O 13 Los nanotextiles exhibieron capacidades reversibles de 326 y 134 mA h g −1 a 20 y 500 mA g −1 , respectivamente, y una capacidad de retención superior al 80% después de 100 ciclos a 500 mA g −1 [2]. Tong y col. fabricado V 6 O 13 cátodo sostenido por una malla de acero con arrugas por el mismo recorrido. El electrodo independiente con una cantidad de carga de V 6 O 13 hasta 2,0 mg cm −2 fue obtenido. A una densidad de corriente de 500 mA g −1 , el V 6 O 13 electrodo demostró una capacidad inicial de 225 mA h g −1 que se deterioró a alrededor de 150 mA h g −1 después de 500 ciclos [21]. Sin embargo, la investigación anterior involucró la electrodeposición en dos pasos y la eliminación de MnO 2 . El crecimiento directo de la nanoestructura de óxido de vanadio de valencia mixta con buenas propiedades electroquímicas sigue siendo un gran desafío [22]. Mientras tanto, estudios previos no han demostrado V 6 O 13 cátodo flexible basado en, que tiene un uso potencial en los dispositivos portátiles.
Aquí, propusimos un proceso hidrotermal simple para hacer crecer con éxito V 6 interconectados O 13 nanohojas sobre el tejido carbonizado para fabricar un electrodo autónomo 3D. Exhibió capacidades específicas de 161 y 105 mA h g −1 a las corrientes específicas de 300 y 1200 mA h g −1 , respectivamente. Con recubrimiento de nanotubos de carbono (CNT) para mejorar aún más su conductividad, sus capacidades específicas aumentaron a 170 y 140 mA h g −1 . Mientras tanto, también se mejoró su rendimiento ciclista. Podría retener el 74% de la capacidad inicial con recubrimiento de CNT, en comparación con el 50% de retención sin recubrimiento de CNT después de 400 ciclos a 300 mA g −1 . La mejora en el rendimiento electroquímico se atribuyó principalmente al efecto sinérgico de la nanoestructura 3D de V 6 O 13 y red conductora jerárquica.
Métodos
Síntesis de c-textile
La tela de bambú disponible comercialmente se empapó en una solución con 2,5 g de NaF y 60 ml de H 2 O durante 1 hy se secó durante 5 h en horno a 120 ° C. El tejido seco se carbonizó a 800 ° C en N 2 durante 30 min para obtener c-textile.
Crecimiento de 3D V 6 O 13 Nanoestructura sobre c-textil
3D V 6 O 13 La nanoestructura se cultivó en c-textile mediante un método hidrotermal asistido por semillas. c-textil se oxidó ligeramente en el ácido nítrico condensado (80% en peso) durante 30 min. V 2 O 5 Se añadió polvo (1 mg) a 5 ml de agua desionizada y luego se sometió a ultrasonidos durante 15 min para obtener una suspensión. El c-textil oxidado se sumergió luego en la suspensión durante 2 h, se secó y se calentó a 300 ° C durante 10 min para hacer crecer la semilla de óxido de vanadio sobre c-textil. V 2 O 5 Se añadió polvo (16 mg) a 224 μl de H 2 al 30% en peso O 2 y se agitó durante 10 min para obtener una solución marrón. Luego se diluyó con 40 ml adicionales de agua destilada y se agitó durante 30 min. Después de que la solución se transfirió a un autoclave de acero inoxidable de 25 ml, el tejido c oxidado se sumergió en la solución. El autoclave se mantuvo a 180 ° C durante 48 h, luego la muestra se lavó con agua destilada y alcohol y se secó a 60 ° C durante 8 h para finalmente obtener el V 6 flexible 3D autónomo. O 13 nanoestructura soportada con c-textil flexible. CNT se revistió adicionalmente en V 6 O 13 nanoestructura sumergiéndola repetidamente en una suspensión de NMP (0,5 mg / ml) de CNT de paredes múltiples y secándola para producir un V 6 O 13 / Electrodo compuesto CNT.
Caracterización de materiales
La morfología del producto se observó mediante microscopía electrónica de barrido (SEM, Philips XL30 FEG) y microscopía electrónica de transmisión (TEM, JEOL JEM-2010). Se realizaron análisis de espectroscopía de fotoelectrones de rayos X (XPS) (K-Alpha) utilizando una fuente monocromática de Al Ka.
Fabricación de baterías y mediciones electroquímicas
Se montaron pilas de botón estándar de tipo CR2016 en una guantera llena de argón (Vigor Inc. Suzhou, China) con V 6 O 13 electrodo como electrodo de trabajo con una carga de masa de ~ 1 mg cm −2 . Se utilizó una hoja de litio como contraelectrodo; 1 mol de LiPF 6 en una mezcla de carbonato de etileno (EC), carbonato de dietilo (DEC) y carbonato de dimetilo (DMC) con una relación de volumen de 1:1:1 se utilizó como electrolito, y se utilizó una película de polipropileno como separador. Las células ensambladas se ciclaron electroquímicamente entre 1,5 y 4,0 V frente a Li / Li + para carga / descarga galvanostática en un sistema de prueba de batería LAND (Wuhan Kingnuo Electronics Co., Ltd., China) a 25 ° C. Se realizaron estudios de espectroscopia de impedancia electroquímica (EIS) con la estación de trabajo Autolab PGSTAT302N en el rango de frecuencia de 10 mHz a 10 kHz.
Resultados y discusión
El esquema del crecimiento de 3D V 6 O 13 nanohojas interconectadas en c-textile se mostró en el archivo adicional 1:Figura S1. El textil (Fig. 1a) se carbonizó en primer lugar a 800 ° C para obtener c-textil (Fig. 1b). Las imágenes SEM (Fig. 2a) mostraron que el c-textil estaba compuesto por haces tejidos de fibras de carbono con un diámetro de ~ 5 μm. c-textile exhibió una excelente flexibilidad y resistencia mecánica. Se pudo enrollar y torcer como se muestra en la Fig. 1c. Se midió que la resistividad cuadrada del tejido c era 5 Ω / sq. con el método de cuatro sondas. Por lo tanto, se utilizó como un prometedor soporte / colector flexible para los materiales de los electrodos. Luego se sumergió en VO x suspensión, se secó y se mantuvo a 300 ° C durante 10 min para hacer crecer los cristales de semillas. Su cambio de peso fue indetectable (<0,1 mg). Después de sumergirlo en óxido de vanadio (VO x ) solución de sol para el crecimiento hidrotermal, el tejido c negro se cubrió con una capa de una película delgada de color amarillo verdoso; sin embargo, se mantuvo su flexibilidad, como se muestra en la Fig. 1d. Su resistividad aumentó a 50 Ω / sq. Las imágenes SEM (Fig. 2b, c) mostraron además que estaba compuesto por nanohojas interconectadas de varios micrones de largo y varios cientos de nanómetros de ancho, como bloques de construcción para construir nanoestructura 3D en c-textile. La imagen TEM de alta resolución (Fig. 2f) mostró franjas de celosía bien definidas de las nanoláminas crecidas. El espaciado de 3.5 Å en la franja de celosía fue consistente con (110) distancia interplanar de la V 6 ortogonal O 13 fase (tarjeta PDF n. ° 71-2235) que estaba de acuerdo con el patrón XRD (Fig. 3c). El mecanismo de crecimiento fue que el cristal semilla se nucleó primero en los sitios con un grupo funcional portador de oxígeno [23, 24]. Luego, durante el proceso hidrotermal en el VO x solución acuosa, interconectada V 6 O 13 Se cultivaron continuamente nanohojas sobre los cristales de semillas. En cuanto a la formación de microflores estructuradas en 3D, podría deberse a los varios cristales de semillas agregados en la misma ubicación para el crecimiento de las nanohojas. Para determinar aún más el estado de valencia del elemento vanadio en V 6 O 13 , Los análisis de XPS se realizaron en el V 6 interconectado sintetizado O 13 nanohojas. El escaneo XPS de la encuesta (Fig. 3a) reveló que la muestra estaba compuesta por elementos V, O, C y N. Las energías de unión para el vanadio 2p3 / 2 y 2p1 / 2 se identificaron en la Fig. 3b a 516.0 y 523.9 eV para V 4+ y 517.3 y 525.0 eV para V 5+ , respectivamente. Fue muy consistente con el estado químico del vanadio en V 6 O 13 informó [25, 26, 27]. Los resultados anteriores confirmaron que 3D V 6 O 13 Las nanoestructuras se cultivaron con éxito en c-textile mediante un simple proceso hidrotermal asistido por semillas.

Imágenes ópticas de a textil disponible comercialmente, b textil carbonizado, c c-textil enrollado y retorcido, y d c-textil con V 6 crecido O 13 en el estado enrollado, recuadro:en el estado plano

Microestructura de V 6 autónomo interconectado 3D O 13 nanohojas en c-textile: a , b imágenes SEM de baja resolución de c-textile sin y con nanohojas, respectivamente; c , d imágenes SEM de alta resolución de nanohojas interconectadas cultivadas en c-textile; e , f imágenes TEM de baja y alta resolución de la nanohoja, respectivamente
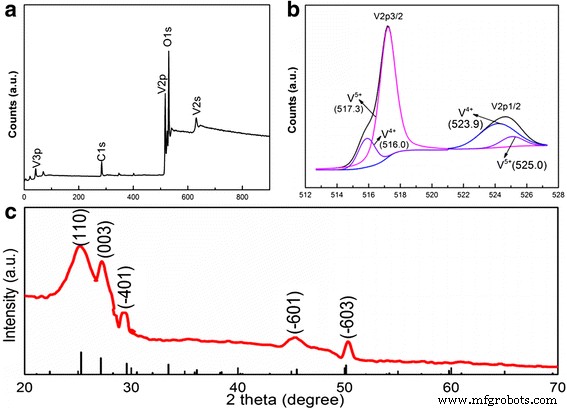
un Un espectro XPS de estudio de V 6 interconectado autónomo en 3D O 13 nanohojas cultivadas en c-textile. b Espectro de V 2p y O 1s con una curva ajustada. c Los patrones XRD de V 6 O 13
Para investigar el rendimiento electroquímico de 3D V 6 O 13 nanoestructuras cultivadas en c-textiles, baterías de moneda de media celda se ensamblaron con un V 6 O 13 electrodo como cátodo y lámina de litio como ánodo. La Figura 4a muestra las curvas típicas de voltametría cíclica (CV) de V 6 O 13 electrodo en una frecuencia de exploración de 0,2 mV s −1 entre 1,5 y 4,0 V (en comparación con Li / Li + ). Los principales picos redox a 2,8 / 2,5 V se pueden identificar fácilmente. También se pudo observar un pico anódico amplio a ~ 3,2 y 2,3 V y un pico catódico a ~ 1,8 V [11, 28]. La aparición de los picos anteriores indicó transiciones de fase de varios pasos, y la ubicación de los voltajes máximos fue consistente con los reportados previamente [2]. La Figura 4b mostró la curva de carga / descarga galvanostática para el primer ciclo a la corriente específica de 30 mA g −1 . Se pudieron identificar múltiples mesetas de voltaje mal definidas. En la curva de descarga, se identificaron dos mesetas inclinadas a 2.3 y 2.8 V, correspondientes a los picos anódicos. Cuando las corrientes específicas aumentaron de 30 a 150, 300, 600 y 1200 mA g −1 , las capacidades específicas fueron 253, 176, 161, 133 y 105 mA h g −1 . Las buenas propiedades electroquímicas se debieron a la nanoestructura 3D compuesta de V 6 O 13 nanohojas. Tal estructura abierta podría entrar muy bien en contacto con los electrolitos y acortar el Li + vía de transporte y difusión. La morfología del V 6 original O 13 electrodo y el electrodo ciclado con SEI se examinó en SEM (archivo adicional 1:Figura S2). La morfología de las nanohojas interconectadas en 3D se mantuvo durante el ciclo. Esto sugiere además la importancia de la nanoestructura 3D en la integridad estructural de V 6 O 13 electrodo durante el ciclo electroquímico. Sin embargo, la conductividad de V 6 O 13 disminuyó a medida que avanzaba la litiación [7, 29]. Además, la longitud de la nanohoja en el V 6 O 13 electrodo alcanzó varias decenas de micrones. Solo una pequeña parte de la nanoplaca individual está conectada directamente con las fibras de carbono conductoras del c-textil, que sirvió como colector. Podría obstaculizar la transferencia de electrones durante el proceso de carga / descarga. Para mejorar aún más la conductividad y, por lo tanto, las propiedades electroquímicas del V 6 autónomo 3D O 13 electrodo, se sumergió en dispersión de CNT para sumergir CNT en su superficie. La Figura 5a, b mostraba imágenes SEM del V 6 O 13 electrodo con CNT. CNT se depositó con éxito en el plano de V 6 O 13 nanosheets y contactamos íntimamente con ellos. Incluso el puente se construyó a través de CNT entre nanohojas vecinas, como se muestra en la Fig. 5c. Como era de esperar, la resistividad del V 6 O 13 electrodo con CNT disminuyó de 50 a 20 Ω / sq. Después del recubrimiento de los CNT, el pico redox apareció en la misma posición en el perfil CV (Fig. 4a) mientras que aumentaron las corrientes pico. Indicó una cinética rápida de reacción electroquímica en V 6 O 13 electrodo con CNT. El V 6 O 13 El electrodo con CNT mostró un mejor rendimiento de velocidad en comparación con el electrodo sin recubrimiento de CNT, como se muestra en la Fig. 4c. Las capacidades de descarga específicas fueron 261, 185, 170, 153 y 140 mA h g −1 a las corrientes específicas de 30, 150, 300, 600 y 1200 mA g −1 , respectivamente, correspondiente a un aumento del 12 ~ 40% en comparación con el cátodo compuesto sin CNT. Para verificar aún más el papel de CNT, calculamos el coeficiente de difusión de iones de litio con voltamperometría cíclica. El V 6 O 13 / Los coeficientes de difusión anódica y catódica CNT fueron 4,79 × 10 −8 y 2,01 × 10 −8 cm 2 s −1 , superior a V 6 O 13 2,42 × 10 −8 del electrodo y 1,7 × 10 −8 cm 2 s −1 , respectivamente (y la discusión asociada está en el archivo adicional 1:Figura S3). Gráficos de Nyquist (Fig. 6a) de V 6 O 13 electrodo y V 6 O 13 El electrodo con CNT mostró formas similares, una forma de semicírculo en el dominio de frecuencia alta a media y una línea inclinada en las regiones de baja frecuencia, correspondiente a la impedancia de reacción electroquímica (proceso de transferencia de carga) y el proceso de difusión de iones de litio. El recuadro es el circuito equivalente utilizado para ajustar las gráficas de Nyquist. En el circuito, CPE es el elemento de ángulo de fase constante y W es la impedancia de Warburg. R s y R ct representan la resistencia óhmica (resistencia total del electrolito, separador y contactos eléctricos) y la resistencia de transferencia de carga, respectivamente [22, 30]. Archivo adicional 1:La Tabla S1 enumeró los parámetros utilizados para ajustar las gráficas. R ct para el V 6 O 13 / El electrodo CNT se calculó en 37,24 Ω, menor que el de V 6 O 13 (55,58 Ω). Esta disminución en la resistencia a la transferencia de carga se atribuyó a la adición de CNT. El mecanismo se ilustró en la Fig. 6b. CNT íntimamente conectado con V 6 O 13 nanohojas para una transferencia de electrones más rápida. Además, los CNT y la fibra de carbono en el tejido c componen una red conductora jerárquica para una mejor conducción de electrones. La ciclabilidad de V 6 O 13 electrodos se muestra en la Fig. 4d. A la corriente específica de 300 mA g −1 , el electrodo con recubrimiento de CNT podría mantener el 74% de la capacidad inicial de 170 mA h g −1 después de 300 ciclos de carga / descarga, mientras que el V 6 O 13 El electrodo solo retuvo el 42% de su capacidad inicial. Superó a la mayoría de los óxidos de vanadio de valencia mixta de baja dimensión o su nanoestructura 3D que se enumeran en el archivo adicional 1:Tabla S2. La mejor ciclabilidad de V 6 O 13 electrodo con CNT podría atribuirse a las siguientes razones:(1) Reforzado con CNT, V 6 O 13 Se mejoraron las propiedades mecánicas. (2) Incluso si V 6 O 13 La nanoestructura se rompió durante el proceso de descarga / carga, todavía estaba unida a CNT y podía activarse electroquímicamente. (3) Autosegregación de V 6 O 13 nanosheets estaba limitado por la aparición de CNT. (4) El recubrimiento de CNT podría ser una barrera válida para aliviar la reacción secundaria del óxido de vanadio con el electrolito, si existe. Por lo tanto, el recubrimiento de CNT puede ser una forma alternativa fácil de mejorar la conductividad de la nanoestructura 3D, aparte del recubrimiento de carbono y el recubrimiento polimérico que generalmente requieren un enorme trabajo de síntesis química [14]. El rendimiento electroquímico general de V 6 O 13 El cátodo estaba limitado por la conductividad de la tela de carbono, la difusividad de Li en V 6 O 13 materiales y transferencia de electrones entre V 6 O 13 nanoestructuras y la tela de carbono. En el trabajo futuro, se pueden realizar mejoras adicionales de las siguientes maneras:(1) reduciendo la resistencia del sustrato de tela de carbono, (2) dopaje V 6 O 13 con azufre para mejorar su difusividad de iones de litio, y (3) recubrir el V 6 O 13 con revestimiento de polímero conductor.
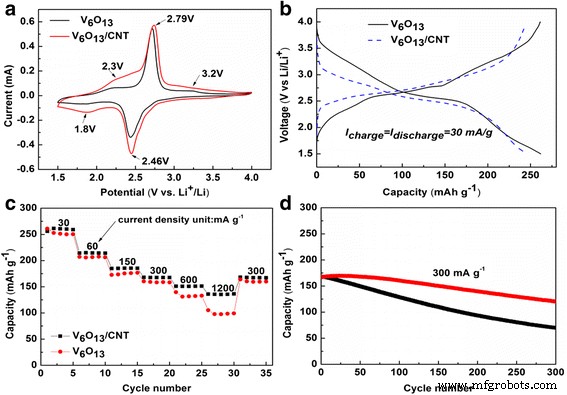
Rendimiento electroquímico de V 6 autónomo 3D O 13 electrodos con / sin recubrimiento de CNT. un Curvas de voltamperometría cíclica. b Curvas de carga / descarga galvanostática. c Calificar. d Rendimiento de ciclabilidad de los dos electrodos

Microestructura de V 6 recubierto de CNT O 13 electrodo. un Imagen SEM de baja resolución del electrodo. b , c Imagen SEM de alta resolución del electrodo que muestra la cobertura de CNT en la nanohoja y un puente entre las nanohojas
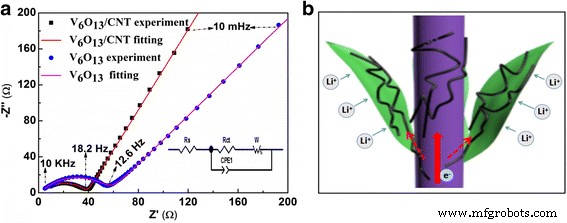
un Gráficos de Nyquist de V 6 O 13 electrodo con / sin recubrimiento de CNT. b Esquema de la ruta de transporte de electrones en V 6 recubierto de CNT O 13 electrodo
Conclusiones
En resumen, fabricamos con éxito V 6 autónomo en 3D O 13 nanoestructura compuesta de nanoláminas interconectadas a través de un proceso hidrotermal facilitado por semillas como cátodo para LIB. El electrodo mostró un buen comportamiento electroquímico. Podría mejorarse aún más recubriendo 3D V 6 O 13 nanoestructura con CNT, superando a la mayoría de los óxidos de vanadio de valencia mixta. Su excelente desempeño se debió a su nanoestructura 3D abierta y su red conductora jerárquica compuesta por CNT en nanoescala y fibra de carbono en microescala. El diseño de nanoestructura 3D con el bloque de construcción (p. Ej., Nanoalambre, nanohoja) combinado con la construcción de la ruta conductora jerárquica mediante recubrimiento de CNT se puede extender a otros materiales de electrodos para un mejor rendimiento electroquímico.
Abreviaturas
- 3D:
-
Tridimensional
- CE:
-
Eficiencia coulombica
- CNT:
-
Nanotubos de carbono
- c-textil:
-
Textil carbonizado
- CV:
-
Voltamperometría cíclica
- DEC:
-
Carbonato de dietilo
- DMC:
-
Carbonato de dimetilo
- EC:
-
Carbonato de etileno
- EIS:
-
Espectroscopia de impedancia electroquímica
- LIB:
-
Batería de iones de litio
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopía electrónica de transmisión
Nanomateriales
- Necesidad de desarrollar un proceso de estandarización de tintes
- Grados PVDF renovables para baterías de iones de litio
- Síntesis fácil de nanopartículas de SiO2 @ C ancladas en MWNT como materiales de ánodo de alto rendimiento para baterías de iones de litio
- Compuesto negro de acetileno / MoS2 de pocas capas como material de ánodo eficiente para baterías de iones de litio
- Efecto de diferentes aglutinantes sobre el rendimiento electroquímico del ánodo de óxido metálico para baterías de iones de litio
- Compuesto de grafeno / Si integrado fabricado por reducción térmica de magnesio como material anódico para baterías de iones de litio
- Un ánodo de película de Fe2O3 nanocristalino preparado por deposición de láser pulsado para baterías de iones de litio
- Cátodos de hojas carbonizados impregnados con selenio independientes para baterías de sodio y selenio de alto rendimiento
- Síntesis de NiCo2O4 similar al erizo de mar mediante una estrategia de autoensamblaje impulsada por carga para baterías de iones de litio de alto rendimiento
- Material de cátodo de alto rendimiento de FeF3 · 0.33H2O modificado con nanotubos de carbono y grafeno para baterías de iones de litio
- Preguntas y respuestas:Optimización de las baterías de iones de litio para una carga extremadamente rápida



