Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
Resumen
Estructura hueca LiNb 3 O 8 Los fotocatalizadores se prepararon mediante un método hidrotermal que ayudaba al proceso de sinterización. La agregación de las partículas para formar estructuras huecas con cavidades obvias puede atribuirse a la volatilización del elemento Li durante el proceso de calcinación. Todos los LiNb 3 O 8 Los polvos muestran una alta eficiencia fotocatalítica de degradación del azul de metileno (MB), especialmente para la muestra calcinada a 700 ° C (LNO700), con solo 3 h para descomponer completamente el MB. La fotodegradación de MB sigue la cinética de pseudoprimer orden y la tasa de primer orden obtenida es 0,97 / h. La mayor tasa de degradación de LNO700 se puede atribuir a su estructura hueca que proporciona una superficie específica más grande y sitios más activos para degradar las moléculas de MB. La prueba cíclica de fotodegradación y adsorción de MB sobre polvo LNO700 indica que la estructura hueca del LiNb 3 O 8 el fotocatalizador es estable y el LiNb 3 O 8 El fotocatalizador es un fotocatalizador eficaz con buena capacidad de reutilización, confirmado por las pruebas de espectroscopía de fotoelectrones de rayos X y XRD antes y después de la fotodegradación de MB.
Antecedentes
En los últimos años, la crisis energética y la contaminación ambiental se han convertido en dos desafíos urgentes, que inhiben gravemente el desarrollo económico y la salud humana. La fotocatálisis se considera la respuesta a ambos problemas, ya que tiene la capacidad de producir hidrógeno y descomponer contaminantes orgánicos. Desde que Fujishima y Honda descubrieron la división fotocatalítica del agua usando TiO 2 como electrodo en 1972 [1], TiO 2 ha sido ampliamente investigado en la degradación de contaminantes orgánicos en el agua. Desde entonces, se estudian varios materiales semiconductores para buscar el fotocatalizador más conveniente con alta eficiencia, bajo costo, respeto al medio ambiente y utilización directa de la luz solar.
Los niobatos, que incluyen principalmente tres grupos:niobatos alcalinos, niobatos de columbita y ortoniobatos de tierras raras, se han estudiado ampliamente en muchas aplicaciones, como dispositivos ópticos, condensadores electrolíticos sólidos, células solares sensibilizadas con colorante y catálisis debido a sus interesantes propiedades físicas y químicas. propiedades [2, 3, 4]. Para las aplicaciones de energía limpia y remediación ambiental, algunos niobatos, como BiNbO 4 [5, 6], LiNbO 3 [7], (Na, K) NbO 3 [8] y LiNb 3 O 8 [9,10,11,12,13,14,15], se han investigado debido a sus estructuras octaédricas de [NbO6] distorsionadas únicas que proporcionan sitios activos para la fotocatálisis. Entre estos materiales, LiNb 3 O 8 se considera un nuevo material de ánodo de batería de iones de litio (LIB) con una gran capacidad teórica de 389 mAh / g, suponiendo transferencias de dos electrones (Nb 5+ → Nb 3+ ) [10, 11]. Como fotocatalizador, LiNb 3 O 8 muestra una producción eficiente de hidrógeno y degradación del contaminante orgánico del azul de toluidina O (TBO) [12,13,14].
El método de preparación convencional de niobatos es la reacción en estado sólido, mientras que siempre da como resultado una distribución no homogénea del elemento Li en la preparación de compuestos Li-Nb-O debido a la fácil volatilización del elemento Li a alta temperatura de recocido. Como máximo, LiNb 3 O 8 se forma fácilmente y se reconoce como una fase de impureza durante la preparación de LiNbO 3 . En comparación con la reacción en estado sólido, el método hidrotermal se usa ampliamente para sintetizar nanomateriales con un tamaño de partícula pequeño, lo que podría proporcionar una superficie específica más grande y sitios más activos en las aplicaciones, especialmente para el proceso fotocatalítico. Las estructuras huecas, siempre acompañadas de excelentes rendimientos, han llamado mucho la atención y se han utilizado en muchos campos, como la catálisis [16]. Se han realizado grandes esfuerzos para mejorar la actividad fotocatalítica de los semiconductores con diversas texturas porosas y huecas, ya que la estructura hueca no solo puede conducir a un área específica más alta sino que también aumenta la eficiencia de captación de luz debido a la dispersión múltiple de la luz [17,18 , 19,20,21,22,23]. Para una estructura hueca LiNb 3 O 8 fotocatalizador, todavía no hay ningún informe anterior y la investigación de LiNb 3 O 8 sigue siendo raro.
En este artículo, la estructura hueca LiNb 3 O 8 Los fotocatalizadores se prepararon mediante el método hidrotermal que ayuda al proceso de sinterización. Se estudiaron sistemáticamente las estructuras cristalinas, las microestructuras y las propiedades ópticas. El rendimiento fotocatalítico de la estructura hueca LiNb 3 O 8 Los fotocatalizadores se evaluaron mediante la degradación del azul de metileno (MB) bajo irradiación con luz ultravioleta.
Métodos
Preparación del fotocatalizador
Estructura hueca LiNb 3 O 8 Los fotocatalizadores se prepararon mediante el método hidrotermal que ayuda al proceso de sinterización utilizando hidróxido de litio monohidrato (LiOH · H 2 O, Aladdin, ACS, ≥ 98,0%) y pentóxido de niobio (Nb 2 O 5 , Aladdin, AR, 99,9%) como materias primas sin purificación adicional. En primer lugar, 3,5 mmol de Nb 2 O 5 se dispersó en 35 ml de agua desionizada con una cierta cantidad de LiOH · H 2 Se añadió O (la relación molar de Li:Nb =8:1) con agitación magnética durante 1 h. Luego, la solución de suspensión se colocó en un reactor autoclave de síntesis hidrotermal revestido con teflón de 50 ml y se mantuvo a 260 ° C durante 24 h. Después de enfriar a temperatura ambiente de forma natural, los polvos blancos obtenidos se centrifugaron, se lavaron con agua desionizada y se secaron. Finalmente, los polvos se calcinaron a varias temperaturas de 600 a 1000 ° C durante 2 h con una velocidad de rampa de 5 ° C / min.
Caracterización
Las estructuras cristalinas de LiNb 3 O 8 Los polvos se analizaron mediante difracción de rayos X en polvo (XRD, Bruker D8 Discover) con radiación Cu Kα. Las morfologías de los polvos se caracterizaron mediante microscopía electrónica de barrido de emisión de campo (SEM, JSM-6700F) y la composición química se midió mediante espectroscopía de rayos X de dispersión de energía (EDS) realizada en SEM. Los espectros de reflectancia difusa UV-vis (DRS) de los polvos se registraron mediante un espectrofotómetro UV-vis-NIR (UV-3600, Shimadzu). Los espectros de fotoluminiscencia (PL) se detectaron usando un espectrofotómetro de fluorescencia Jasco FP-6500. El área de superficie específica se midió en un aparato de área de superficie (Micromeritics ASAP 2460) a 77 K por N 2 método de adsorción / desorción (método BET). El análisis de espectroscopía de fotoelectrones de rayos X (XPS) se realizó en un instrumento Thermo-Fisher Escalab 250Xi.
Pruebas catalíticas
Evaluar el rendimiento fotocatalítico de la estructura hueca LiNb 3 O 8 fotocatalizadores, la degradación de la solución acuosa de MB (10 mg / L) se llevó a cabo bajo la irradiación de una lámpara de 500 W de Hg a un valor de pH natural. Se dispersaron cincuenta miligramos de polvos en 50 ml de solución acuosa MB. Antes de la irradiación, la suspensión se mantuvo en la oscuridad durante 1 h con agitación para lograr el equilibrio de adsorción. Luego, se irradió la suspensión con la lámpara de Hg y se analizó la concentración residual de MB usando UV-3600 a 665 nm con un intervalo de 1 h. Además, el carbono orgánico total (TOC) de la mezcla se determinó mediante el uso de un sistema analizador elementar de TOC alto para investigar si el tinte está completamente degradado.
Para detectar la especie activa durante la reactividad fotocatalítica, los electrones (e - ), agujeros (h + ), radicales hidroxilo (· OH) y el radical superóxido (O 2 · - ) se investigaron añadiendo AgNO 3 5 mM (un extintor de e - ), EDTA-2Na (un extintor de h + ), alcohol terc-butílico ( t -BuOH, un extintor de · OH) y benzoquinona (BQ, un extintor de O 2 · ), respectivamente. El método fue similar al anterior ensayo de actividad fotocatalítica.
Resultados y discusión
Los patrones XRD de LiNb 3 O 8 los polvos calcinados a diferentes temperaturas durante 2 h se muestran en la Fig. 1. Como se ve en la figura, a 600 ° C, las fases principales son LiNbO 3 y Nb 2 O 5 , sin LiNb 3 O 8 fase observada en absoluto. A 700 ° C, la fase predominante es LiNb 3 O 8 , con una pequeña cantidad de LiNbO 3 residual , que significa LiNb 3 O 8 se prepara más fácilmente mediante el método hidrotermal que ayuda al proceso de sinterización que los métodos convencionales [10, 11]. Con el aumento de la temperatura de calcinación, solo la fase pura LiNb 3 O 8 se observa y la fase es estable incluso hasta 1000 ° C; además, una temperatura de calcinación más alta significa una mejor cristalinidad y un tamaño de grano más grande. Como se muestra en la figura, la fase es perfectamente consistente con la tarjeta JCPDF no. 36-0307 (insertado en la Fig. 1 como referencia), que está indexado a la fase monoclínica, un grupo espacial de P21 / a.
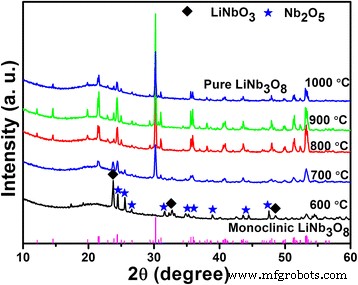
Patrones XRD del LiNb 3 O 8 polvos calcinados a diferentes temperaturas durante 2 h
Las imágenes SEM de LiNb 3 O 8 Los polvos calcinados a diferentes temperaturas se muestran en la Fig. 2. Puede verse claramente que a 700 y 800 ° C, las partículas se agregan para formar estructuras huecas con cavidades obvias. Se puede atribuir a la volatilización del elemento Li durante el proceso de calcinación, que es beneficiosa para la formación de nuevos LiNb 3 O 8 partículas y redes entre las partículas [15]. Al mismo tiempo, los sitios de conexión y las formas de las partículas parecen indistintos en la muestra a 700 ° C debido a su escasa cristalinidad. Con el aumento de la temperatura de calcinación, el tamaño de grano aumenta de ~ 100 nm a 700 ° C a 1 ~ 3 μm a 1000 ° C; las formas de las partículas se vuelven más obvias con una cristalinidad mejorada; las cavidades se vuelven cada vez menos y la estructura hueca casi desaparece a 1000 ° C. Como sabemos, un tamaño de partícula pequeño siempre significa una gran superficie específica. Tanto el área de superficie específica alta como una buena cristalinidad son factores importantes que afectan la actividad fotocatalítica, por lo que se debe lograr un compromiso [4]. La composición química medida por EDS se muestra en la Fig. 2e. Muestra la presencia de elementos C, O y Nb en el LiNb 3 sintetizado O 8 polvos, ya que el elemento Li es indetectable.
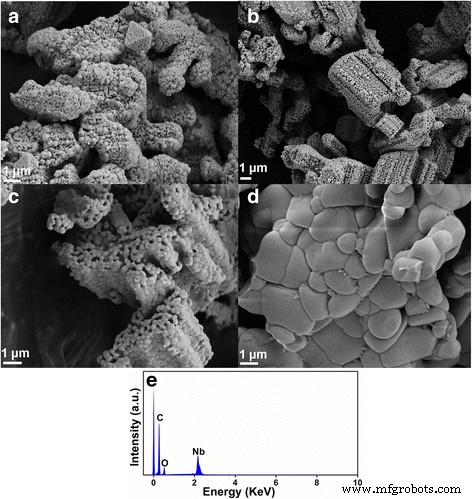
Imágenes SEM de LiNb 3 O 8 polvos calcinados a a 700 °, b 800 °, c 900 ° y d 1000 ° C, respectivamente. e Espectro EDS de LiNb 3 O 8 polvos
Las propiedades ópticas de la estructura hueca LiNb 3 O 8 también se midieron los polvos. Los espectros de absorbancia de reflectancia difusa UV-vis de LiNb 3 O 8 los polvos se registran en la Fig. 3. Usando un BaSO 4 prensado polvo como referencia, el coeficiente de absorbancia ( α ) se obtiene a partir de los espectros de reflectancia difusa basados en la teoría de Kubelka-Munk (K-M). Como LiNb 3 O 8 es el semiconductor de banda prohibida directa [12], la banda prohibida ( E g ) se puede calcular de acuerdo con la relación entre el borde de absorción y la energía del fotón (hv) escrito de la siguiente manera:
$$ \ alpha \ mathrm {h} v =A {\ left (\ mathrm {h} v- {E} _g \ right)} ^ {\ frac {1} {2}} $$ (1)donde A es la constante de absorbancia de los semiconductores. La banda prohibida de LiNb 3 O 8 Los polvos calcinados a 700 °, 800 °, 900 ° y 1000 ° C (indicados como LNO700, LNO800, LNO900 y LNO1000, respectivamente) se estiman en 3,74, 3,78, 3,76 y 3,71 eV, respectivamente, más pequeños que los intervalos de banda informados. antes [12, 14]. Significa LiNb 3 O 8 los polvos solo pueden absorber la luz ultravioleta durante el proceso fotocatalítico.
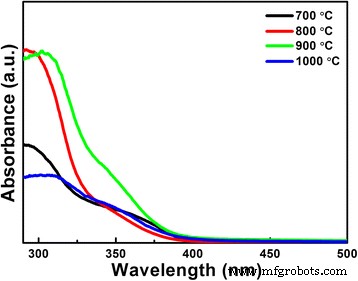
Espectros de absorbancia de reflectancia difusa UV-vis de LiNb 3 O 8 polvos
La eficiencia de separación de los transportes fotogenerados del LiNb 3 O 8 Los fotocatalizadores se investigan mediante espectros PL, como se muestra en la Fig. 4. Se puede ver claramente que para LiNb 3 O 8 fotocatalizadores, la intensidad del pico de emisión de PL se debilita gradualmente. Como el pico de emisión de PL más alto siempre corresponde a la combinación más fácil de portadores, el LiNb 3 O 8 El fotocatalizador exhibe una mejor eficiencia de separación de huecos de electrones fotogenerados en la superficie con el aumento de la temperatura de calcinación, lo que puede atribuirse a la cristalinidad mejorada con un crecimiento obvio del tamaño de grano. Especialmente para LNO1000, su tamaño de grano es de varios micrómetros, bastante diferente de otros tres de estructura hueca LiNb 3 O 8 polvos. Aunque aumenta la temperatura de calcinación más alta, que puede mejorar la eficiencia de separación de los transportes fotogenerados, también se produce una gran reducción del área de superficie específica, que es uno de los factores más importantes que influyen en la eficiencia fotocatalítica. Las áreas BET de LNO700, LNO800, LNO900 y LNO1000 son 10,7, 4,46, 0,36 y 0,23 m 2 / g, respectivamente; el área de superficie más grande de LNO700 y LNO800 resulta de la estructura porosa y hueca.
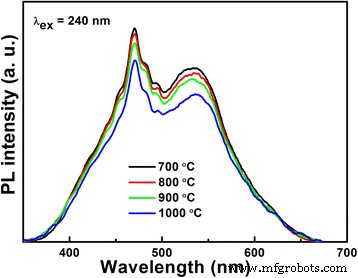
Espectros PL de temperatura ambiente del LiNb 3 O 8 fotocatalizadores
El rendimiento fotocatalítico de LiNb 3 O 8 Los polvos se evalúan mediante la degradación de MB bajo irradiación con luz ultravioleta, como se ilustra en la Fig. 5. Antes de la irradiación, se alcanza el equilibrio de adsorción / desorción en la oscuridad para investigar la capacidad de adsorción. Muestra que los polvos LNO700 y LNO800 muestran una buena capacidad de adsorción, alrededor del 14 y 10%, respectivamente, mientras que sólo el 3% para LNO900 y LNO1000; la capacidad de adsorción es consistente con las morfologías de los fotocatalizadores que se muestran en la Fig. 2. En comparación con la degradación de MB sin fotocatalizador, todos los LiNb 3 O 8 los polvos muestran la mayor eficiencia fotocatalítica de degradación de MB, especialmente para LNO700, con solo 3 h para descomponer completamente MB. Y el% de TOC de la misma muestra tomada después de un tiempo de reacción de 3 h muestra una eliminación del 83% de los carbonos orgánicos del tinte. La diferencia entre C / C 0 y el valor de TOC% está relacionado principalmente con la presencia de intermedios no degradables. Significa LiNb 3 O 8 los polvos son fotocatalizadores eficientes en la degradación de contaminantes orgánicos. La eficacia fotocatalítica de LiNb 3 O 8 Los catalizadores se clasifican en orden de mayor a menor:BNO700> BNO800> BNO900> BNO1000. Se puede observar que con el aumento de la temperatura de calcinación, la capacidad de degradación fotocatalítica disminuye, lo que se puede atribuir al cambio de morfología de LiNb 3 O 8 polvos:las estructuras huecas con cavidades evidentes van desapareciendo gradualmente. Por lo tanto, las estructuras huecas juegan el papel más importante en el proceso de degradación, que proporcionan una superficie específica más grande y sitios más activos para degradar las moléculas de MB. Para LNO700, el mejor rendimiento fotocatalítico también puede atribuirse al efecto sinérgico entre LiNb 3 O 8 y LiNbO 3 . Estas dos formas de niobato pueden interactuar entre sí, y los electrones fotogenerados pueden evitar la recombinación de manera más eficiente [14].
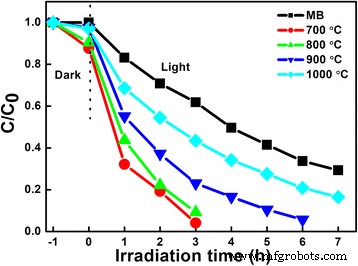
Fotodegradación de MB con respecto al tiempo de irradiación usando LiNb 3 O 8 polvos expuestos a la luz ultravioleta. Capacidad de absorción de LiNb 3 O 8 los polvos se prueban después de agitar durante 1 h en la oscuridad para lograr la adsorción en equilibrio
La constante de velocidad de primer orden ( k ) también se calcula para exhibir la capacidad fotocatalítica de LiNb 3 O 8 polvos basados en el modelo cinético de Langmuir-Hinshelwood modificado [24], como se muestra en la Fig. 6. El k obtenido son 0,18, 0,97, 0,75, 0,45 y 0,25 / h para MB, LNO700, LNO800, LNO900 y LNO1000, respectivamente. La tasa aparente también muestra que LNO700 con una estructura hueca es el fotocatalizador más eficiente entre ellos, aproximadamente 4 veces más alto que el de LNO1000 y 5,5 veces más alto que el de MB sin un fotocatalizador.
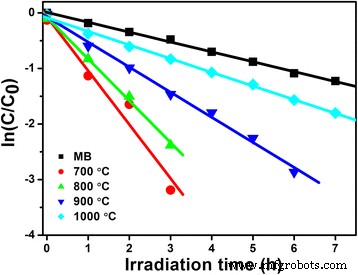
Ajuste cinético para la fotodegradación de MB en presencia de LiNb 3 O 8 polvos calcinados a diferentes temperaturas
Investigar la reutilización y estabilidad de la estructura hueca LiNb 3 O 8 fotocatalizador (LNO700) para la degradación fotocatalítica y la capacidad de adsorción de MB, se realizan cinco ciclos de fotodegradación de MB, como se muestra en la Fig. 7a, b. Después de cinco ciclos de fotodegradación de MB, no se muestra ninguna pérdida de rendimiento evidente con la descomposición completa de MB en 3 h. Al mismo tiempo, en primer lugar estudiamos la estabilidad de la capacidad de adsorción de LNO700 y los resultados muestran que para cada ciclo, la adsorción de MB en la oscuridad casi puede mantenerse constante. Indica que la estructura hueca del LiNb 3 O 8 El fotocatalizador es estable, lo que garantiza que el LiNb 3 O 8 El fotocatalizador con estructuras huecas es un fotocatalizador eficiente con buena reutilización para aplicaciones prácticas.
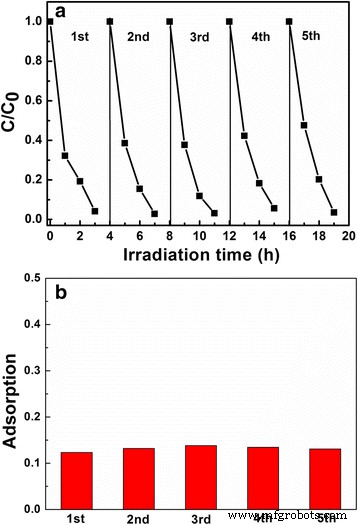
Ciclismo a fotodegradación y b adsorción de MB sobre polvo LNO700
La Figura 8 muestra el experimento de captura de especies activas durante el proceso de reacción fotocatalítica con catalizadores LNO700. Se puede ver que la degradación de MB obviamente disminuye con la adición de AgNO 3 (un extintor de e - ), t -BuOH (un extintor de · OH) y BQ (un extintor de O 2 · ). Por el contrario, la degradación aumentó con la adición de EDTA-2Na (un extintor de h + ), lo que significa que se promueve la separación de electrones y huecos y se generan más electrones. Por tanto, se puede concluir que e - , · OH y O 2 · son las principales especies activas en el proceso de degradación en lugar de h + . En el proceso fotocatalítico, los electrones fotogenerados (e - ) en la transferencia de la banda de conducción a la superficie del LiNb 3 O 8 fotocatalizador y reducir el oxígeno molecular al anión superóxido (O 2 · ); entonces, el anión superóxido puede reaccionar con H 2 O para formar los radicales activos (· OH) [25, 26]. Estas reacciones finalmente resultarían en la degradación de MB.
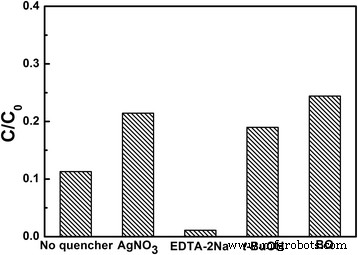
Experimento de captura de especies activas durante la degradación de MB bajo irradiación de luz ultravioleta con presencia de LiNb 3 O 8 catalizadores
Para investigar la fotocorrosión del LiNb 3 O 8 fotocatalizador, LNO800 se caracteriza por XRD y XPS antes y después de la fotodegradación de MB, como se muestra en las Figs. 9 y 10. Los resultados de XRD muestran que las estructuras cristalinas del LiNb 3 O 8 El fotocatalizador varió insignificantemente después de su uso, siendo LiNb 3 puro O 8 sin impurezas evidentes. Sin embargo, en los espectros XPS, los picos de Nb3d se desplazan a una energía de enlace más baja en comparación con el LiNb 3 no utilizado O 8 , lo que indica que parcialmente, Nb 5+ se ha reducido y la fotorreducción de LiNb 3 O 8 ocurrió en la superficie durante el proceso de fotodegradación [15, 27,28,29].
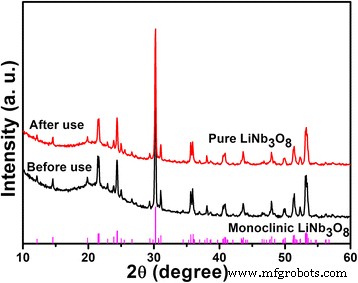
Patrones XRD de fotocatalizadores LNO800 antes y después de la fotodegradación de MB bajo irradiación UV
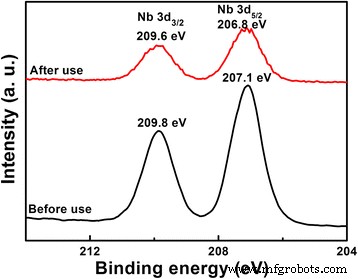
Espectros XPS de Nb3d para fotocatalizadores LNO800 antes y después de la fotodegradación de MB bajo irradiación UV
Conclusiones
La estructura hueca LiNb 3 O 8 Los fotocatalizadores se prepararon mediante el método hidrotermal que ayuda al proceso de sinterización. La agregación de las partículas para formar estructuras huecas con cavidades obvias puede atribuirse a la volatilización del elemento Li durante el proceso de calcinación. Todos los LiNb 3 O 8 Los polvos muestran una alta eficiencia fotocatalítica de la degradación de MB, especialmente para LNO700, con solo 3 h para descomponer completamente MB. La fotodegradación de MB sigue la cinética de pseudoprimer orden, y la tasa de primer orden obtenida es 0,97 / h. La mayor tasa de degradación de LNO700 se puede atribuir a su estructura hueca que proporciona una superficie específica más grande y sitios más activos para degradar las moléculas de MB. La prueba cíclica de fotodegradación y adsorción de MB sobre polvo LNO700 indica que la estructura hueca del LiNb 3 O 8 el fotocatalizador es estable y el LiNb 3 O 8 El fotocatalizador es un fotocatalizador eficiente con buena reutilización para aplicaciones prácticas, confirmado por las pruebas XRD y XPS antes y después de la fotodegradación de MB.
Nanomateriales
- C Estructura y Función
- Diferencia entre estructura y unión.
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Estrategia de sinterización asistida por hidrotermia hacia material de ánodo LiNb3O8 de estructura hueca y porosa
- Alto rendimiento fotocatalítico de dos tipos de fotocatalizadores compuestos de TiO2 modificado con grafeno
- Los efectos de la relación Li / Nb en la preparación y el rendimiento fotocatalítico de los compuestos Li-Nb-O
- Rendimiento fotocatalítico de luz visible de nanocompuestos de ZnO / g-C3N4 dopado con N
- Preparación de micromateriales híbridos de MnO2 recubiertos de PPy y su rendimiento cíclico mejorado como ánodo para baterías de iones de litio
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2



